Xuelin Xia, Xiaoyuan Yang, Wei Huang, Xiaoxia Xia*, Deyue Yan*
Nano-Micro Letters (2022)14: 33
https://doi.org/10.1007/s40820-021-00762-9
2. 该纳米胶束Z-M ADCN在HER2阳性的卵巢癌和乳腺癌模型中显示出优异的抗肿瘤性能,可以消除体积约为100 mm³和500 mm³的实体瘤,其肿瘤抑制率达99.8%,并且该纳米药物在体内具有很好的生物安全性。
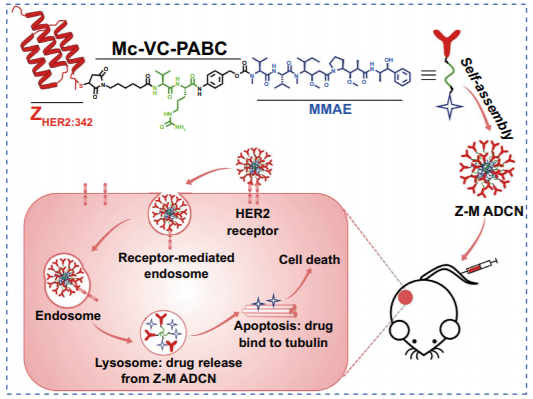
为解决以上问题,上海交通大学颜德岳教授课题组和夏小霞教授课题组,提出采用亲和体蛋白与疏水药物毒素偶联制备亲和体-药物偶联物并采用自组装策略制备主动靶向纳米药物以改善ADC药物的不足。因亲和体-药物偶联物ZHER2:342-MMAE的两亲性质使其在水溶液中成功组装形成120 nm左右的纳米胶束,组装后的纳米胶束依然保持亲和体蛋白的高亲和性能。在HER2阳性卵巢癌(SKOV-3)和乳腺癌(BT474)肿瘤模型小鼠中,Z-MADCN纳米药物在两种肿瘤模型中均获得优异的抗肿瘤性能,肿瘤抑制率高达99.8%,小鼠的肿瘤全部被治愈无复发,并且纳米药物在小鼠体内具有很高的生物安全性。
亲和体蛋白N端的巯基与海图毒素的Linker马来酰亚胺基团通过迈克尔加成方法制备亲和体-药物偶联物ZHER2:342-MMAE,该偶联物的分子量为8438.14。在水溶液中该偶联物自组装形成胶束大小为120 nm左右的胶束结构。自组装形成纳米胶束Z-M ADCN依然保持了ZHER2:342亲和体的高亲和性,其亲和性大小约为6.44×10⁻⁹ M。

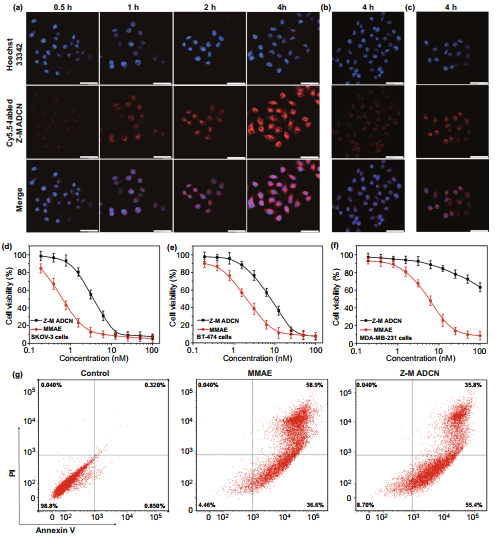
II Z-M ADCN体外性能评价
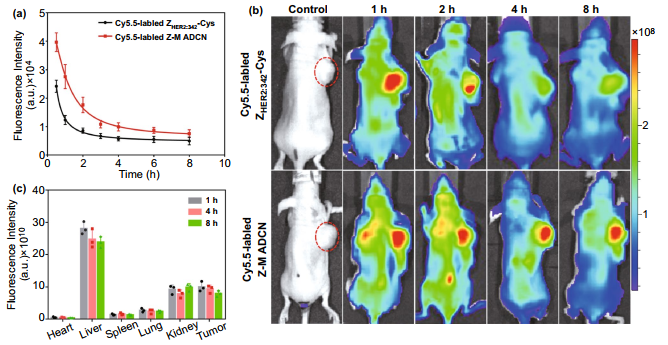
亲和体分子因其分子量较小,容易在体内清除。相较于亲和体,自组装形成的Z-M ADCN具有一定的纳米尺寸,有利于延长在体内的血液循环时间。基于此,我们采用SD大鼠研究Z-M ADCN在体内的药代动力学情况。结果表明Z-MADCN在体内的清除速率明显降低,其体内半衰期明显长于ZHER2:342亲和体在体内的半衰期。进一步地,在近红外荧光成像中显示Cy5.5标记的Z-M ADCN更容易在肿瘤部位富集,且在肿瘤部位滞留时间明显增长。这些结果证明Z-M ADCN具有巨大的靶向治疗潜力。
IV Z-M ADCN在SKOV-3及BT474荷瘤小鼠中的抗肿瘤性能
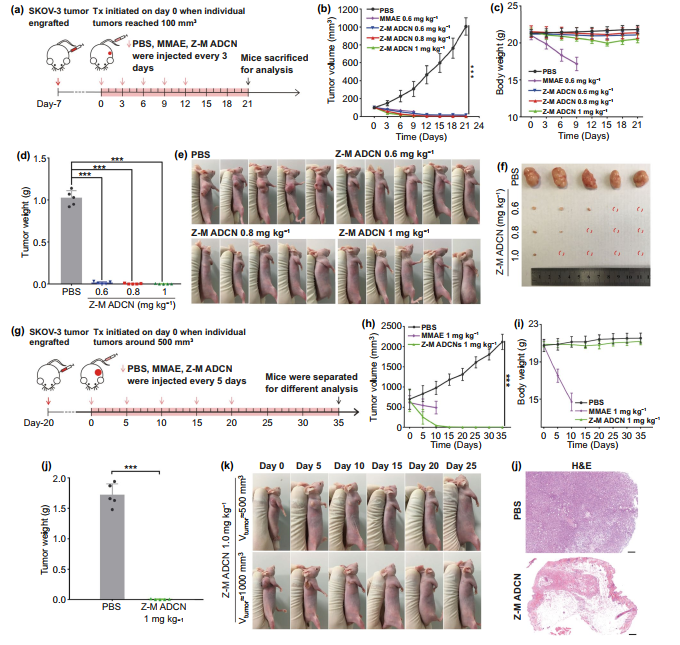
图4. Z-M ADCN对SKOV-3肿瘤的体内抗肿瘤效果。(a) Z-M ADCN对对肿瘤体积为100 mm³ SKOV-3荷瘤小鼠的治疗过程;(b, c) SKOV-3荷瘤小鼠治疗过程中体积及体重的变化曲线图;(d, e, f) Z-M ADCN治疗结束后的种瘤体重,治疗结束后小鼠照片及肿瘤照片;(g, h, i) Z-M ADCN对对肿瘤体积为500 mm³ SKOV-3荷瘤小鼠的治疗及给药后肿瘤体积和体重的变化曲线;(j, k, l) 治疗结束后的肿瘤质量,治疗过程中小鼠照片及治疗结束后各组肿瘤组织的H&E染色照片。
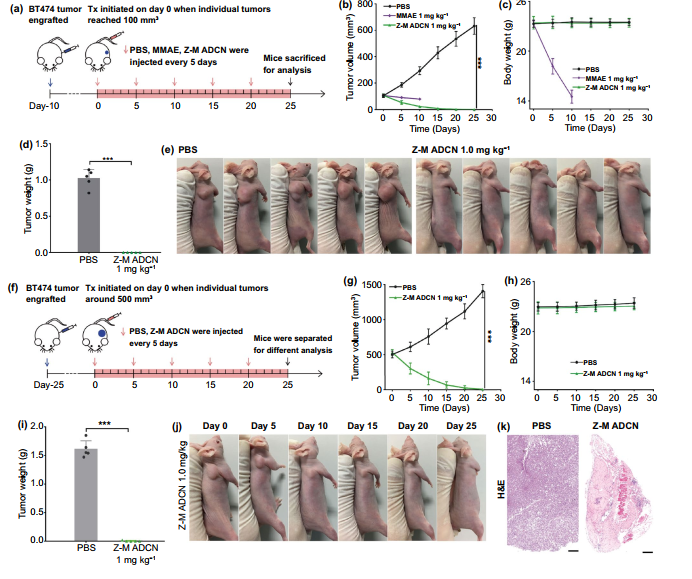
图5. Z-M ADCN对BT474肿瘤的体内抗肿瘤效果。(a) Z-M ADCN对对肿瘤体积为100 mm³ BT474荷瘤小鼠的治疗过程;(b, c) BT474荷瘤小鼠治疗过程中体积及体重的变化曲线图;(d, e) Z-M ADCN 治疗结束后的种瘤体重,治疗结束后小鼠照片;(f, g, h) Z-M ADCN对对肿瘤体积为500 mm³ BT474荷瘤小鼠的治疗及给药后肿瘤体积和体重的变化曲线; (i, j, k) 治疗结束后的肿瘤质量,小鼠照片及H&E染色照片。
 夏雪霖
夏雪霖
本文第一作者
上海交通大学 博士研究生
靶向蛋白-药物偶联物纳米药物的制备研究。
 夏小霞
夏小霞
本文通讯作者
上海交通大学 教授
蛋白材料合成生物学研究。
▍主要研究成果
▍Email: xiaoxiaxia@sjtu.edu.cn
 颜德岳
颜德岳
本文通讯作者
上海交通大学 教授
超分子自组装和抗肿瘤新药研制。
▍主要研究成果
▍Email: dyyan@sjtu.edu.cn

Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 颜德岳院士等:亲和体-药物偶联物自组装纳米药物靶向治愈卵巢癌和乳腺癌
 Nano-Micro Letters
Nano-Micro Letters 王中林院士和王杰研究员等:MXene 水溶液润滑的长寿命高电流密度摩擦伏特纳米发电机
王中林院士和王杰研究员等:MXene 水溶液润滑的长寿命高电流密度摩擦伏特纳米发电机 NML2023.11封面文章丨北大吕万良等:生物正交工程化病毒样纳米粒用于高效基因治疗递送
NML2023.11封面文章丨北大吕万良等:生物正交工程化病毒样纳米粒用于高效基因治疗递送 NML综述 | 多功能钙钛矿光电探测器—从分子尺度结构设计到微/纳米尺度形貌调控
NML综述 | 多功能钙钛矿光电探测器—从分子尺度结构设计到微/纳米尺度形貌调控