Antiangiogenesis-Combined Photothermal Therapy in the Second Near-Infrared Window at Laser Powers Below the Skin Tolerance Threshold
Nano-Micro Lett.(2019)11:93
https://doi.org/10.1007/s40820-019-0327-4
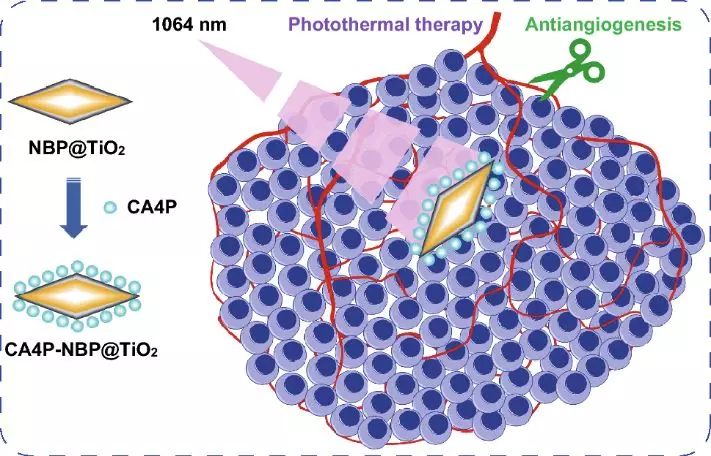
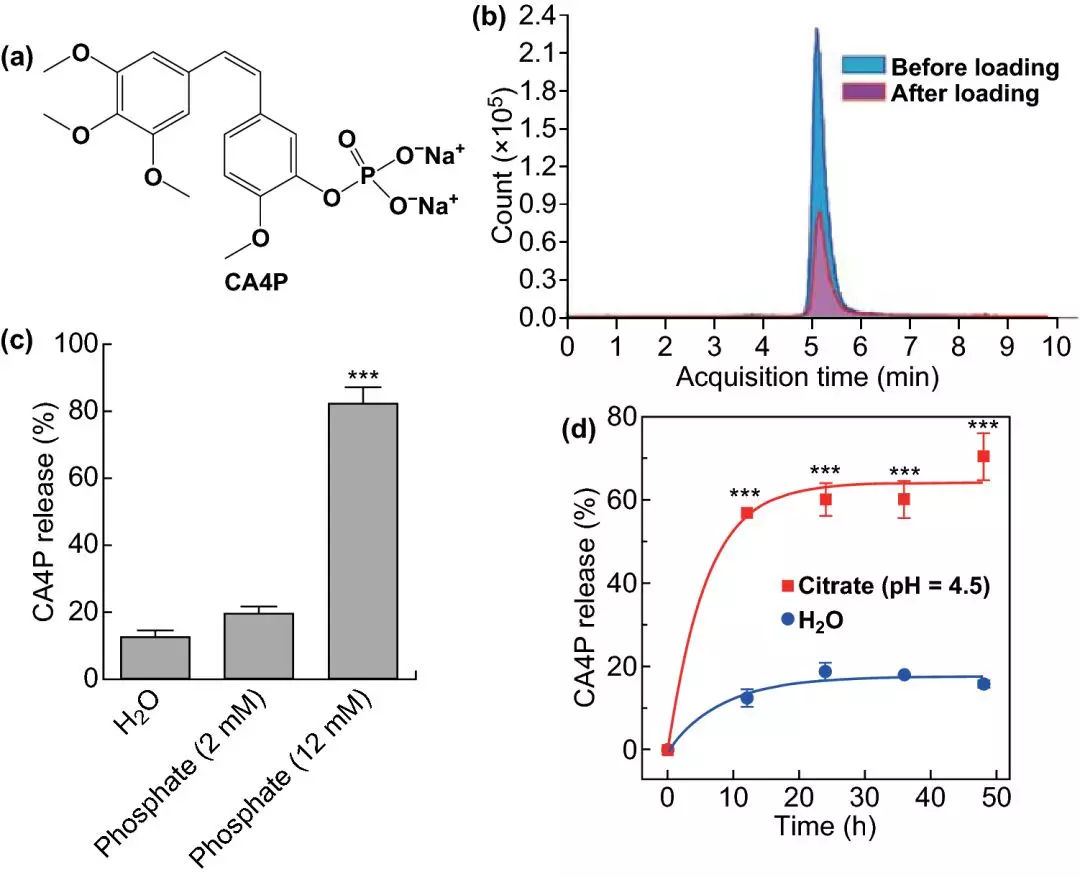
2 二氧化钛外壳能够装载抗癌药物combretastatin A-4 phosphate(CA4P)。
3 在低于皮肤耐受阈值的激光功率密度下,负载CA4P的NBP@TiO2纳米颗粒在1064 nm激光照射下发挥协同抗血管生成和抗肿瘤作用。
NBP@TiO2被用作NIR-II区的PTT介导材料和抗肿瘤药物CA4P的载体。合成的NBP@TiO2纳米材料具有1064 nm的纵向等离子体共振吸收峰,在1064 nm激光照射下该材料具有很高的光热转换效率,这确保其在NIR-II区发挥理想光热效应。同时该纳米材料具有良好的生物相容性。此外,TiO2涂层作为CA4P的有效载体,能够实现CA4P和热量的同时输送。在人肺癌A549细胞和人脐静脉内皮细胞(HUVECs)中观察到光热治疗和化疗联用的协同抗肿瘤和抗肿瘤血管生成效果。体内动物实验中也发现这种联用能有效抑制肿瘤微血管密度和肿瘤细胞增殖。
研究背景
利用种子介导生长法制备Au NBP,并纯化。然后以TiCl3为前体,水解生成TiO2包覆NBP。TEM结果显示其平均长度为116.9 ± 1.1 nm,宽度为32.9 ± 0.3 nm。TiO2包覆的平均厚度为16.6 ± 0.4 nm。NBP纳米颗粒的纵向等离子体共振吸收波长为970 nm。TiO2涂层导致吸收峰红移到1064 nm,这使得NBP@TiO2纳米颗粒成为响应NIR-II窗口的PTT试剂。根据其升温曲线以及功率与平台温度的关系,在1064 nm激光的照射下,该材料的光热转换效率高达(93.3 ± 5.2)% 。

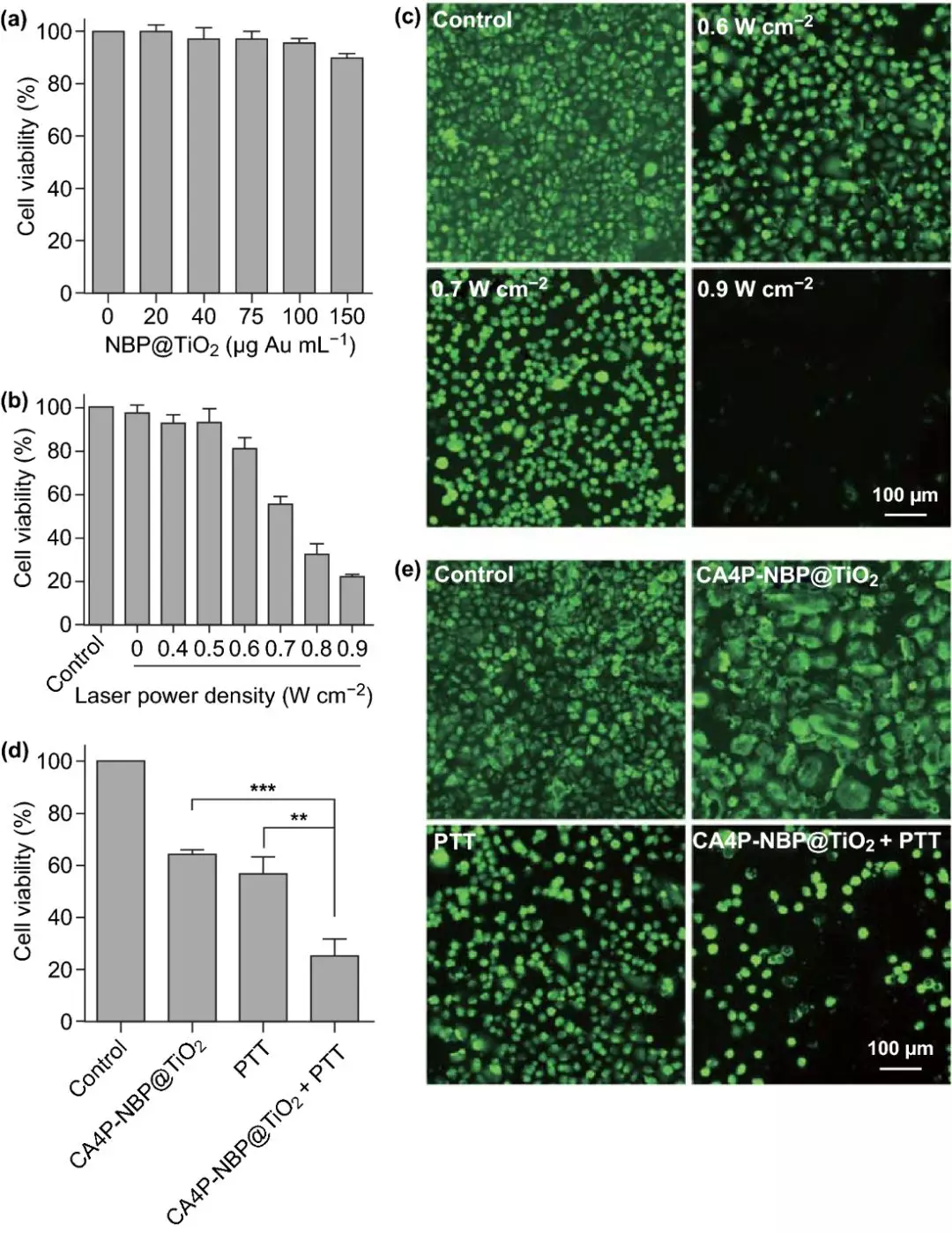
III 在A549细胞中的PTT研究
IV PTT对人脐静脉内皮细胞(HUVECs)活性以及微管蛋白的影响
与单独治疗相比,负载CA4P的NBP@TiO2纳米颗粒和PTT的联用治疗对HUVECs产生更加明显的细胞毒性,且联用后细胞内微管蛋白分布发生紊乱。
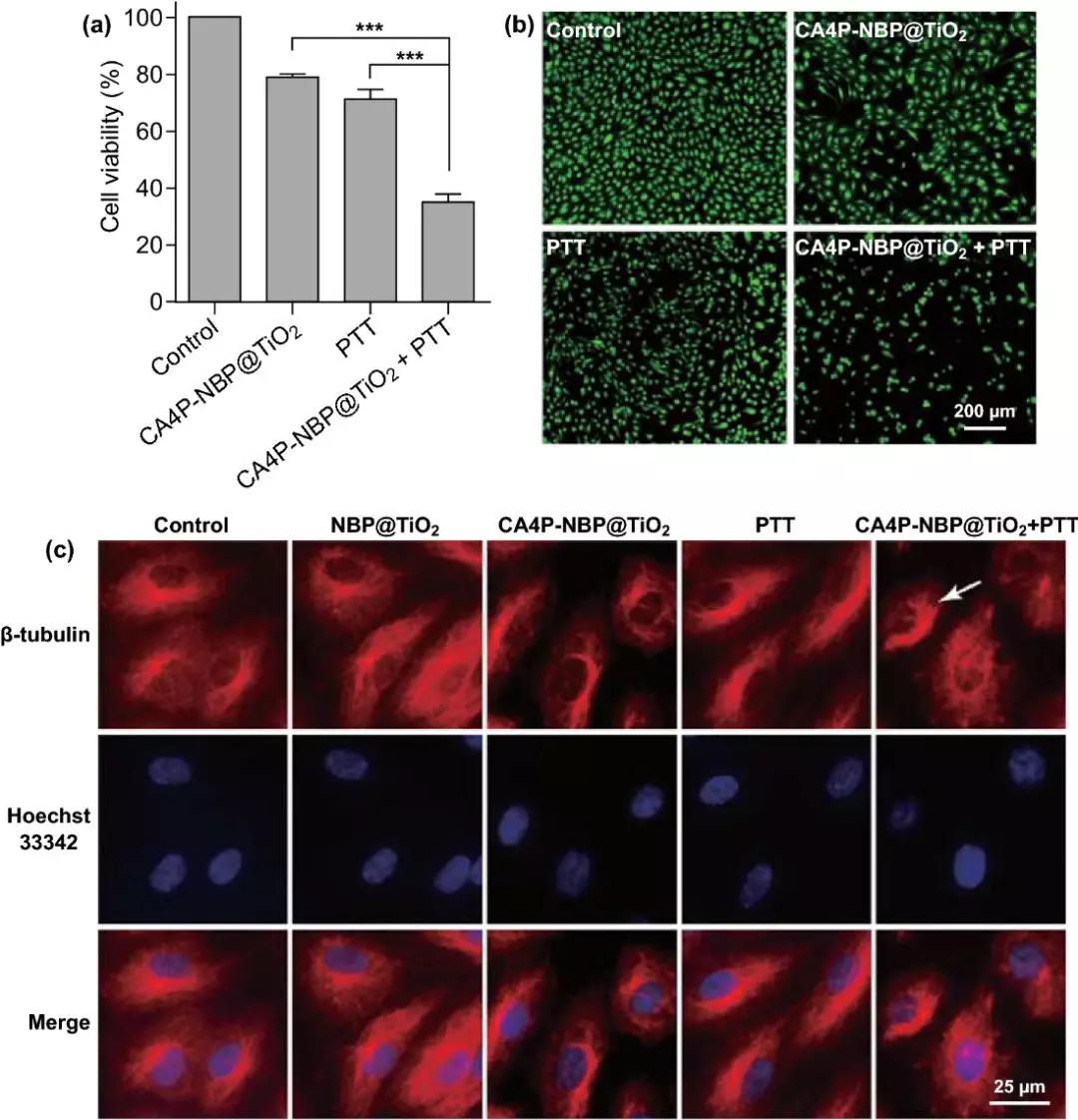
图4 负载CA4P的NBP@TiO2纳米颗粒联用PTT对HUVECs产生协同毒性。(a)MTT分析, (b)calcein AM染色, (c)微管蛋白分布。
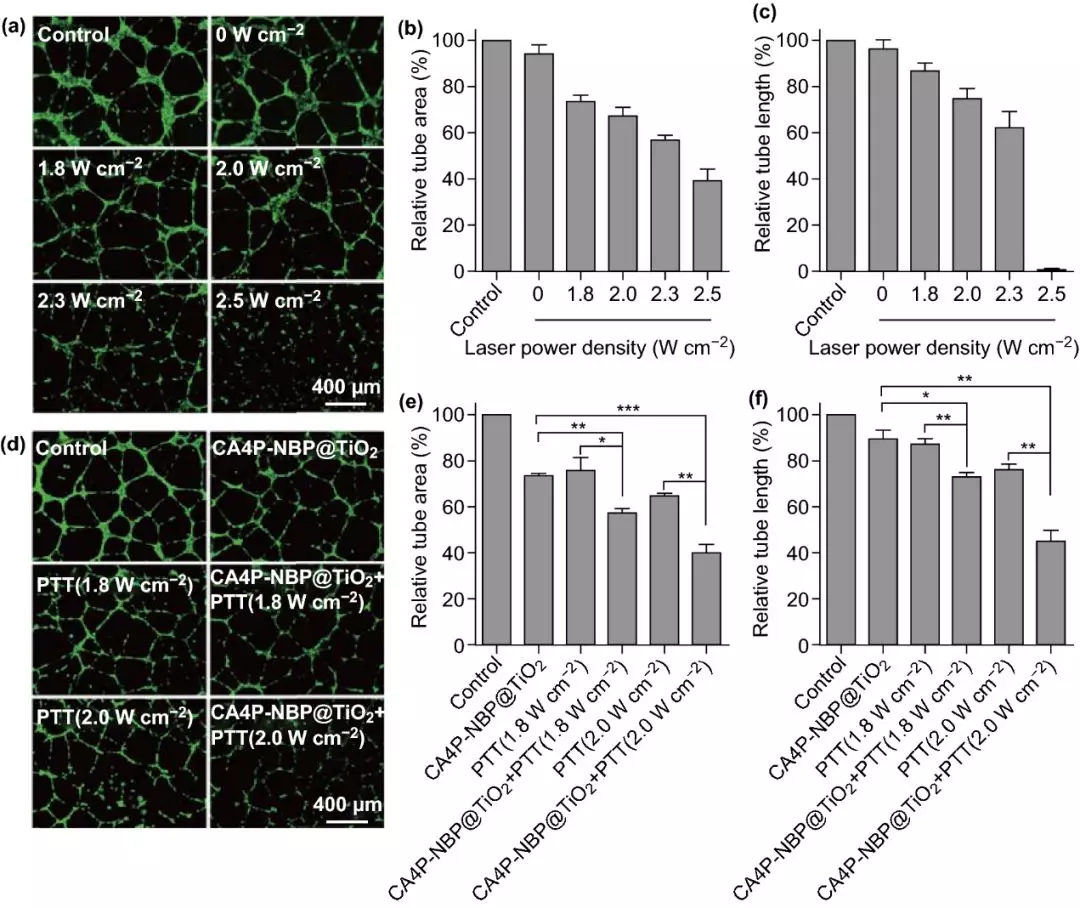
V PTT增强CA4P的抗血管生成作用
肿瘤发展和转移的一个关键步骤是血管生成,它为细胞提供营养和氧气,并清除废物。低剂量(7 nm CA4P,12μg-Au/mL)的CA4P负载NBP@TiO2纳米颗粒轻微抑制HUVECs在Matrigel中形成网状的血管结构,相对血管面积和长度分别为(73.7±1.0)%和(89.6 ± 3.8)%。低功率密度(1.8或2.0 W/cm2)激光照射能提高负载CA4P的NBP@TiO2纳米颗粒的血管生成抑制效应。当载药颗粒与1.8 W/cm2的激光照射联用后,血管面积和长度分别为(57.5± 2.0)%和(73.2 ± 1.8)%。这两个值在2.0 W/cm2激光照射下分别降低到(40.1 ± 3.6)%和(45.2 ± 4.6)%。
 王建方
王建方
(本文通讯作者)
香港中文大学
▍主要成果与荣誉
▍Email: jfwang@phy.cuhk.edu.hk
 竺晓鸣
竺晓鸣
(本文通讯作者)
澳门科技大学
▍主要成果与荣誉
▍Email: xmzhu@must.edu.mo
撰稿:《纳微快报》编辑部
审核:原文作者
编辑:《纳微快报》编辑部
E-mail:editorial_office@nmletters.org
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 高效光热治疗:香港中文大学王建方&澳门科技大学竺晓鸣合作提出肿瘤治疗新方法
 Nano-Micro Letters
Nano-Micro Letters 哈佛大学陶伟等:癌症诊疗的光子纳米药物-超低温剥离的2D锡纳米片
哈佛大学陶伟等:癌症诊疗的光子纳米药物-超低温剥离的2D锡纳米片 复旦大学王建新:一石四鸟—基于人参皂苷的新型多功能肿瘤靶向治疗脂质体
复旦大学王建新:一石四鸟—基于人参皂苷的新型多功能肿瘤靶向治疗脂质体 封面文章|崔大祥教授团队:荷载纳米探针的iPS干细胞用于癌症的光动力和免疫联合治疗
封面文章|崔大祥教授团队:荷载纳米探针的iPS干细胞用于癌症的光动力和免疫联合治疗 快速储钾新材料设计及其机理剖析:烯碳铠甲保护的TiO2纳米管电极的原位表征与DFT理论分析
快速储钾新材料设计及其机理剖析:烯碳铠甲保护的TiO2纳米管电极的原位表征与DFT理论分析