研究背景
电化学水分解制氢为绿氢的可持续生产提供了有效途径。其阳极析氧反应(OER)催化剂通常在碱性环境中表现较好,而酸性条件更适合阴极析氢反应(HER)进行,这两个半反应的pH不匹配严重阻碍了电解槽的工业制氢生产效率。钌基纳米材料在OER和HER方面都显示出巨大的潜力,且价格相对其他铂族金属要便宜得多,因此是理想的全解水催化剂之一。Ru金属对氢的亲和力与Pt相当,具有很好的产氢性能,但是在OER过程中,Ru的过度氧化会产生可溶性的Ruⁿ⁺物质,导致性能显著降低。因此,迫切需要设计和制备双功能钌基电催化剂用于酸性条件下的全水解反应,以实现高效稳定的水分解制氢。
Durable Ru Nanocrystal with HfO₂ Modification for Acidic Overall Water Splitting
Xiangkai Kong*, Jie Xu, Zhicheng Ju*, Changle Chen*
Nano-Micro Letters (2024)16: 185
https://doi.org/10.1007/s40820-024-01384-7
本文亮点
1. 以二氧化铪为基体,采用分级退火制备了钌铪协同的纳米晶异质结构。
2. 二氧化铪修饰和构筑小晶畴结构的协同作用显著缓解了钌在OER过程中的过度氧化溶解现象。
内容简介
研究证明在OER过程中,Ru在高氧化电位下是不稳定的,容易被氧化到更高价态的Ruⁿ⁺,从而逐渐溶解。因此,构建稳定抗氧化的Ru纳米晶体在全解水反应中具有巨大的潜力,可以同时实现持续且高效的产氧和产氢过程。中国矿业大学孔祥恺/鞠治成团队与中国科学技术大学陈昶乐教授合作,提出了通过加入具有抗氧化性的客体材料来缓解Ru的过度氧化,并制备得到具有小晶畴结构的Ru纳米晶,通过引入HfO₂来减轻Ru的氧化程度。电化学测试结果表明,所制备的催化剂在酸性OER条件下需要197 mV的过电位达到10 mA cm⁻2的响应电流密度,并且在250 h的工作时间内具有稳定的性能。同时,HER性能得到提高,使其成为一种稳定高效的酸性全水解电催化剂。
图文导读
I S-Ru/HfO₂和L-Ru/HfO₂催化剂的合成路径及表征
图1A为S-Ru/HfO₂和L-Ru/HfO₂催化剂的合成示意图,将一定量的Ru(acac)₃和Hf(acac)₄与KBr混合退火,得到含Ru和Hf的纳米片,称为S-Ru/HfO₂。随后通过洗涤和退火来调控结晶性,得样品表示为L-Ru/HfO₂。图1B透射电镜(TEM)展示S-Ru/HfO₂是清晰的二维纳米片结构。图1(C)高分辨率透射电镜(HRTEM)显示原子排列为无序状态,选区电子衍射(SAED)图中观察到的衍射环也与之对应。这些结果表明了S-Ru/HfO₂的非晶结构。TEM(图1E)图像显示L-Ru/HfO₂片状形态保持良好,HRTEM图像中出现了晶体条纹(图1F),晶格间距为0.325和0.236 nm分别对应正交HfO₂ (002) 和六边形Ru (100) 晶体平面。同时,图1(G)所示的衍射环证实了L-Ru/HfO₂中Ru和HfO₂结晶度的提高。图1H S-Ru/HfO₂上的元素分布不均,而图1I L-Ru/HfO₂上的元素分布均匀,这些比较都说明了分级退火对异质界面微观结构的有效修饰。紧密的界面相互作用可以确保Ru和HfO₂的结构稳定性,并在使用过程中提升材料的耐久性。
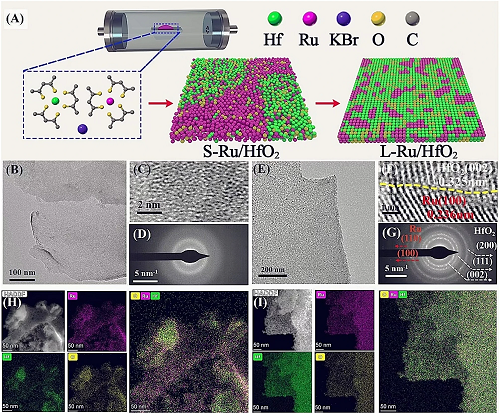
图1. (A)L-Ru/HfO₂催化剂的合成示意图。S-Ru/HfO₂的表征: (B) TEM和(C) HRTEM图像,(D) SAED模式。L-Ru/HfO₂表征: (E) TEM和(F) HRTEM图像,(G)SAED模式。(H) Ru /HfO₂和(I)Ru /HfO₂的HAADF-STEM图像和相应的EDX元素映射。
II Ru与HfO₂相互作用示意及表征
图2A是Ru与HfO₂相互作用示意图,如左侧所示,非晶材料中的无序排列会导致同类型原子和不同种类原子之间的弱相互作用;对于大尺寸的Ru晶体,只是边缘的Ru原子受到界面作用,而其内部Ru原子几乎不受影响(图2A中间图);当结晶畴明显减小,大部分Ru原子可以被HfO₂保护使其具有更高的抗氧化性和抗腐蚀性(图2A右侧图)。HRTEM表征表明,所有生成的Ru和HfO₂晶域小于5 nm(图2B)。拉曼光谱(图2C)分析显示纯Ru纳米片(L-Ru和S-Ru)在491.7、621.8和681.5 cm⁻1处有三个峰,分别对应于Ru-O的Eg、A1g和B2g振动模式。L-Ru的这些峰的强度比S-Ru的要强得多,这表明纯Ru对氧的高敏感性。这些振动峰在S-Ru/HfO₂和L-Ru/ HfO₂上几乎消失,这表明HfO₂的掺入可以有效地阻止Ru金属的氧化。X射线衍射光电子能谱(XPS)记录的L-Ru/HfO₂的测量光谱显示484.4和462.3 eV处的峰分别对应于Ru 3p1/2和Ru 3p3/2(图2D)。S-Ru的Ru⁰/Ruᵟ⁺比值为1.97, 退火后显著降低至0.91 (L-Ru)。相比之下,该比值从S-Ru/HfO₂(2.09)到L-Ru/HfO₂(2.15)的变化小的多。如图2E所示,X射线吸收近边结构(XANES)分析表明,S-Ru/HfO₂的Ru K边处于商用Ru箔和RuO₂之间,表明Ru处于Ru⁰和Ru⁴⁺之间,而L-Ru/HfO₂表现出比S-Ru/HfO₂更明显的吸收边负移,这归因于Ru和HfO₂之间的相互作用更强。同时,可以观测到L-Ru/ HfO₂比S-Ru/ HfO₂具有更多的金属Ru态和更少的Ru-O键(图2G和2H),表现出更好的抗氧化性。
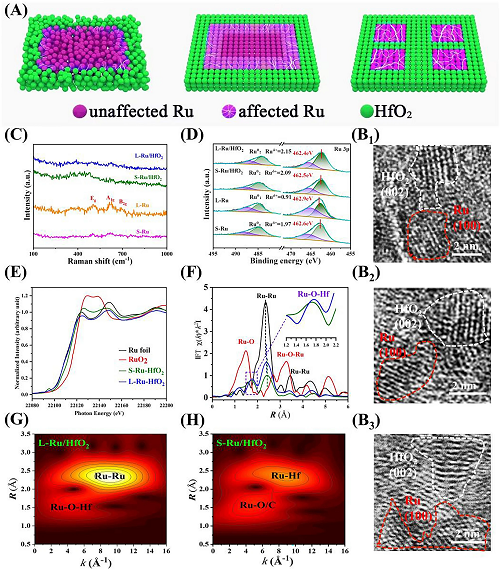
图2. (A)Ru与HfO₂相互作用示意图。(B) L-Ru/HfO₂的HRTEM图像。样品的物理表征: (C)拉曼光谱,(D)Ru 3p轨道高分辨率XPS光谱,(E) XANES光谱,(F) Ru K-edge EXAFS光谱,(G) L-Ru/HfO₂和(H) S-Ru/HfO₂的WT-EXAFS光谱。
III 催化剂的电化学性能和机理分析
电化学测试显示L-Ru/HfO₂在这些催化剂中表现出最小的起始电位(图3A),达到10 mA cm⁻2电流密度所需过电位仅为197 mV。所记录的i-t曲线如图3B所示,L-Ru/HfO₂表现出更好的稳定性。纯Ru催化剂在1.47 V附近有一个明显的氧化峰(图3C),这是由于在外加氧化电位的驱动下Ru向高价态Ru(V)或Ru(VI)持续氧化所致。当与HfO₂结合时,S-Ru/HfO₂的氧化峰明显正移至1.60 V。此外,在L-Ru/HfO₂上,该峰变得无特征,证实了HfO₂的保护赋予小晶畴Ru增强的抗氧化作用,与图3D中电极表面所观察到的情形一致。除此之外,L-Ru/HfO₂在1 M KOH和1 M PBS电解质中性能优于包括RuO₂在内的所有对照样品(图3E)。在酸性环境下,L-Ru/HfO₂的HER性能有明显提升(图3F)。KSCN的实验证明Ru是OER和HER的活性位点(图3G)。当组装成电解槽时,L-Ru/HfO₂需要1.57和1.67 V的电压达到100和300 mA cm⁻2的电流密度,优于其它对比样(图3I)。上述结果证实了这种双功能催化剂的高效稳定表现,展现了一定的实际应用潜力。
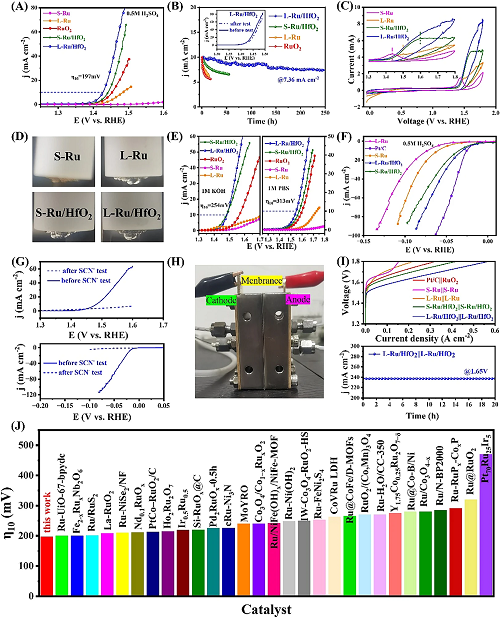
图3. 在0.5 M H2SO4溶液中,三电极体系中样品的电化学测量: (A)为LSV曲线,(B)为10mA cm⁻2时的i-t响应计时电流测量,记录了前后的LSV极化曲线,(C)为OER活化过程中第一次CV扫描。(D)在每个样品激活的第一个CV扫描周期中观察到的电极表面的照片。(E)这些样品在1.0 M KOH和1.0 M PBS中测量的OER LSV曲线。(F)在0.5 M H2SO4溶液中测量这些样品的HER的LSV曲线。(G)涉及电解质的KSCN中OER和HER操作时LSV曲线的比较。(H)组装后的PEM电解槽的图像。(I)L-Ru/HfO₂ / L-Ru/HfO₂耦合PEM电解槽上的极化曲线及耐久性测试。(J)L-Ru/HfO₂上酸性OER的η₁₀与最近报道的Ru基催化剂的比较。
IV 原位拉曼和准原位XPS表征
图4A显示L-Ru/HfO₂上187.9 cm⁻1处的拉曼峰归属于Ru-Ru结合振动,而未经HfO₂修饰的L-Ru在该信号上表现为无特征(图4B),表明了L-Ru/HfO₂中的大部分Ru原子保持着金属态,但L-Ru的Ru原子,特别是表面的Ru原子更倾向于处于氧化态。L-Ru/HfO₂的Ru-Ru峰随着电位的增加逐渐向正方向移动(图4C)。当外加电位高于1.0 V时,Ru-Ru结合峰减弱并负移。即使达到1.6 V,也能在记录的光谱中分辨出该键信号,这表明L-Ru/HfO₂在OER电位窗口区具有稳健的Ru⁰状态,HfO₂修饰显著增强了Ru的抗氧化能力,从而提高了其稳定性。609.8、1198.2和798.8 cm⁻1处的振动谱分别对应M-OH、M-O和M-OOH的结合模式,其中“M”代表催化剂的活性位点(图4C和图4D)。与L-Ru相比,L-Ru/HfO₂表现出相对稳定的M-OH谱,不受电位变化的影响。这表明L-Ru/HfO₂具有稳定的化学环境和结构,可以从水分子的解离中持续供应OH,确保持久的氧气产生。当施加2.0 V氧化电压时,L-Ru/HfO₂的Ru 3p轨道没有发生明显变化(图4E)。然而,S-Ru/HfO₂发生了0.8 eV的移动(图4F)。这说明小晶畴的调控使Ru具有更强的抗氧化能力,使其在OER过程中保持良好的金属态,缓解被过度氧化。
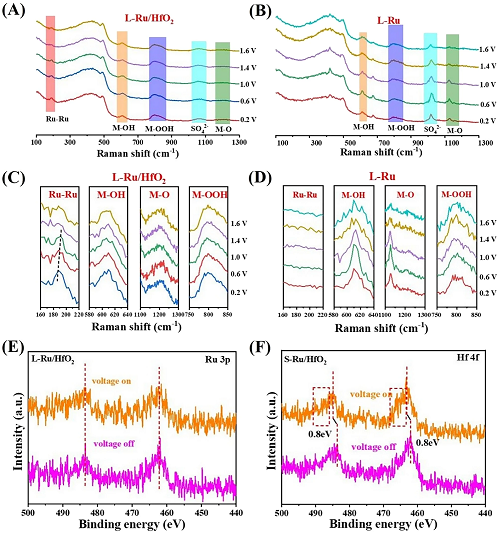
图4. 在(A) L-Ru/HfO₂和(B) L-Ru上记录的原位拉曼光谱。(C) (D)分别为图(A)和图(B)对应振动区域的放大谱。(E) L-Ru/HfO₂和(F)S-Ru/HfO₂在2.0 V电压下Ru 3p信号的准原位高分辨XPS光谱。
V 密度泛函计算
L-Ru/ HfO₂中的Ru活性位点主要保持在金属态,排除了晶格氧途径,因此我们在接下来的讨论中主要关注氧吸附机制(AEM)和双位点机制(DSM)(如图5A),相应的自由能变化图如图5B所示,DSM表现出较小的能垒。差分电荷密度计算揭示了界面处的电子转移,Ru位点的电荷密度聚集与XPS观测结果一致(图5C)。d带中心计算表明HfO₂的存在使d带中心位置从-2.54 eV降至-2.86 eV,距离费米能级更远。同时,Ru/HfO₂对H2O分子的吸附能明显强于纯Ru和RuO₂(图5E)。图5F显示,L-Ru/HfO₂在水蒸气环境下羟基峰明显增加,而L-Ru对水蒸气吸附的响应较小。这些结果表明,HfO₂修饰使得Ru在酸性环境下具有更强的对水吸附能力,有利于水分子在催化剂表面的吸附和解离,保证了产氧的持续进行。此外,过渡态的计算表明,HfO₂的修饰显著减小了Ru解离水分子的能垒(图5G),从而促进酸性OER的进行。
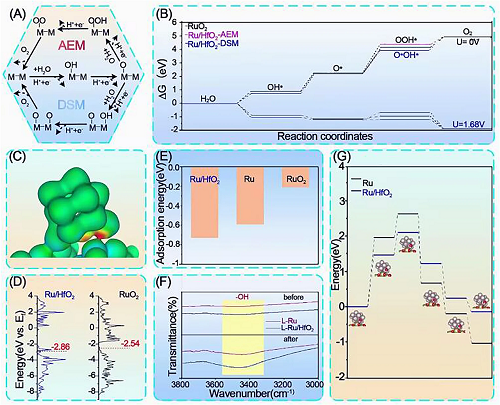
图5. DFT计算。(A)OER在催化剂表面的AEM和DSM路径。(B)不同路径Ru/HfO₂催化剂上OER的自由能变化图。(C) Ru/HfO₂界面电荷密度差,其中暖色表示电荷积累,冷色表示电荷消耗。(D)计算的投影DOS,突出显示活性部位的D波段中心。(E)水分子在这些催化剂上的吸附能。(F)水蒸气处理前后L-Ru和L-Ru/HfO₂的FTIR谱图。(G)解离能图(附图:相应优化的Ru/HfO₂水解离中间态结构。
VI 总结
综上所述,本文通过分级退火法制备了HfO₂修饰的小晶畴Ru纳米晶,对于酸性OER,仅需197 mV过电势就可以达到10 mA cm⁻2的电流密度,并且表现出良好的稳定性。当作为双功能催化剂与质子交换膜组装时,电解槽达到100和300 mA cm⁻2的电流密度所需要的电压分别为1.57 V和1.67 V。电子态研究表明,HfO₂修饰和小晶畴结构的协同作用赋予Ru较低的氧化态,使其具有更强的抗氧化能力。
作者简介

本文通讯作者
主要进行功能纳米材料的设计和研发,并探索其在催化、电磁波吸收、电池回收等领域的应用研究。
▍Email:xkong@cumt.edu.cn

本文通讯作者
主要从事煤基碳材料、介观尺度无机材料的可控组装及电化学储能研究。
▍Email:juzc@cumt.edu.cn

本文通讯作者
烯烃聚合、催化剂制备和废旧塑料利用。
▍Email:changle@ustc.edu.cn
关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2022JCR影响因子为 26.6,学科排名Q1区前5%,中科院期刊分区1区TOP期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 中科大陈昶乐等:HfO₂稳定Ru纳米晶实现酸性环境下高效稳定的全水解制氢
 Nano-Micro Letters
Nano-Micro Letters 宁波材料所王静刚&丁纪恒等:可再生、可加工的坚固聚酯纳米复合材料,用树枝状MXene基异质结原位催化合成
宁波材料所王静刚&丁纪恒等:可再生、可加工的坚固聚酯纳米复合材料,用树枝状MXene基异质结原位催化合成 南方科大曾林等:电解液引入电子受体添加剂实现高电压锂金属电池
南方科大曾林等:电解液引入电子受体添加剂实现高电压锂金属电池
 北航胡明俊&北京纳米能源所杨军等:超稳定/高比能量/宽温域水系碱性钠离子电池通过采用微孔 C₄N/rGO 阳极实现
北航胡明俊&北京纳米能源所杨军等:超稳定/高比能量/宽温域水系碱性钠离子电池通过采用微孔 C₄N/rGO 阳极实现