内容简介
表皮生长因子受体(EGFR)的突变辅助诊断,在酪氨酸激酶抑制剂靶向癌症的治疗中,被认为具有至关重要的作用。有效识别少量的EGFR-突变细胞是当前临床治疗的迫切需求。但是,这些突变细胞信号往往被大部分正常细胞的噪声信号所掩盖,妨碍了突变细胞的有效识别。
国家纳米科学中心胡志远、魏泽文教授等人提出一种基于微流控芯片的方法,有效实现了EGFR的多重突变在单细胞水平的检测。利用微免疫荧光成像技术轻易识别出EGFR-表达细胞,这些单细胞被放置于特别设计的硅微米通道内。同时,通过单细胞的原位裂解,对EFGR-表达细胞的分解物进行进一步监测,避免交叉污染。这项研究证实,微流控芯片技术不仅可以检测是否存在EFGR突变,而且能提供很多其他单细胞级别的信息:比如具体到哪个细胞发生突变,以及同一细胞是否存在多重突变等等。本研究提出的微流控芯片技术将推动简便廉价的DNA Sanger测序成为肿瘤靶向治疗前的常规测试。
文章发表于Nano-Micro Letters期刊2018年第10卷第1期,详情请阅读全文,可免费获取。本文也在微信(nanomicroletters)、微博(纳微快报NML)、科学网博客、Facebook、Twitter等期刊新媒体推出,请大家多关注和阅读。早期的微信推文请关注网站(http://nmsci.cn)。
文章题目:Identifying EGFR-Expressed Cells and Detecting EGFR MultiMutations at Single-Cell Level by Microfluidic Chip
关键词:EFGR突变,单细胞分析,微流芯片,酪氨酸激酶抑制剂
引用信息:Ren Li . Mingxing Zhou . Jine Li . Zihua Wang . Weikai Zhang . Chunyan Yue. Yan Ma. Hailin Peng. Zewen Wei . Zhiyuan Hu, Nano-Micro Lett. (2018) 10: 14. https://doi.org/10.1007/s40820-017-0168-y
图文导读
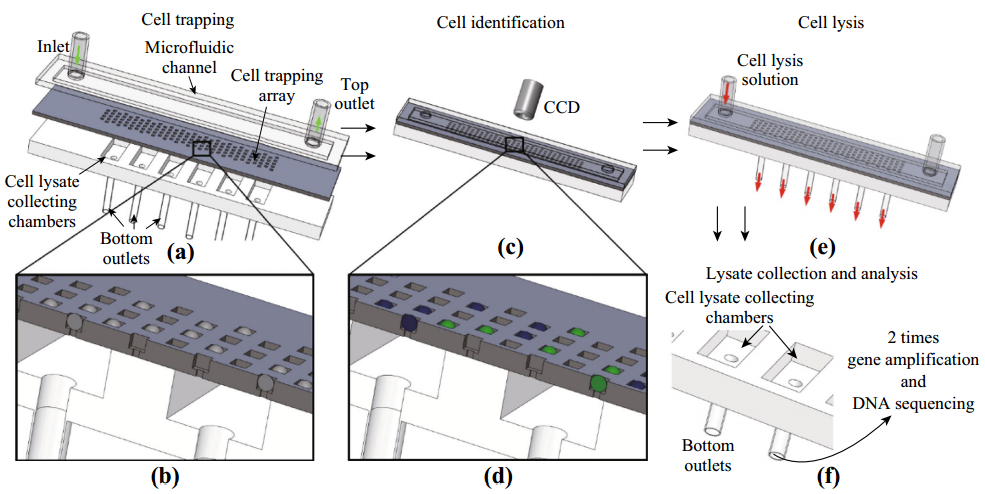
图1:微流控芯片原理及其操作图,a) 细胞混合物被吸入一个微流体芯片,它由三个层次组成:微流体通道、细胞捕获阵列和细胞裂解物收集室。流速为3微升每分钟;b) 细胞进入微孔,方形微孔设计适合于只有一个细胞;c) 芯片荧光检测特定蛋白符号的细胞;d) 蓝色球代表阴性的细胞,呈现出只有DAPI蓝色荧光,而绿色球代表阳性细胞,表现出绿色FITC和DAPI蓝色;e) 微孔的细胞裂解通过微流体通道输入细胞裂解液,细胞裂解液直接作用于细胞裂解液收集室;f) 细胞裂解液分别从细胞裂解物收集室收集,用于DNA扩增和测序。
为了清楚地显示芯片结构,示意图不遵循精确的井数和尺寸。
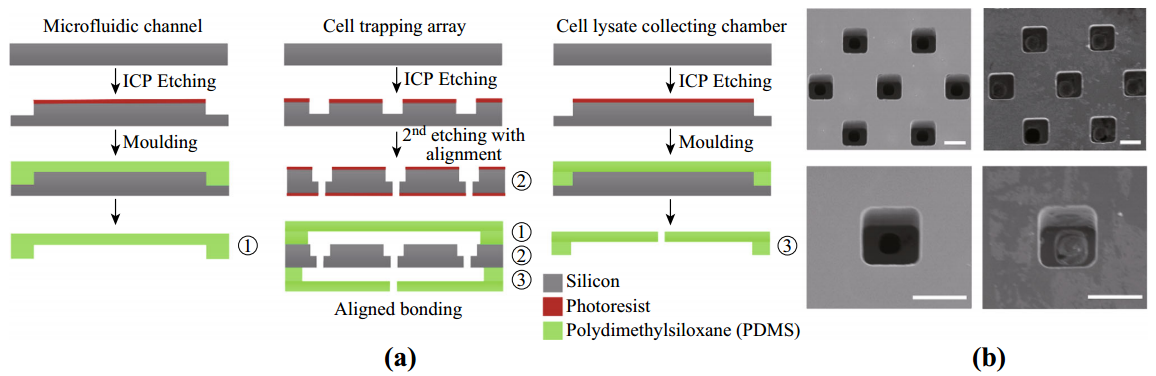
图2:微流控芯片的制作。a)由三层组成的微流控芯片的制作工艺,分别用数字1, 2和3表示, b)空硅微孔(左栏)和单细胞占据微孔(右列)的SEM图像
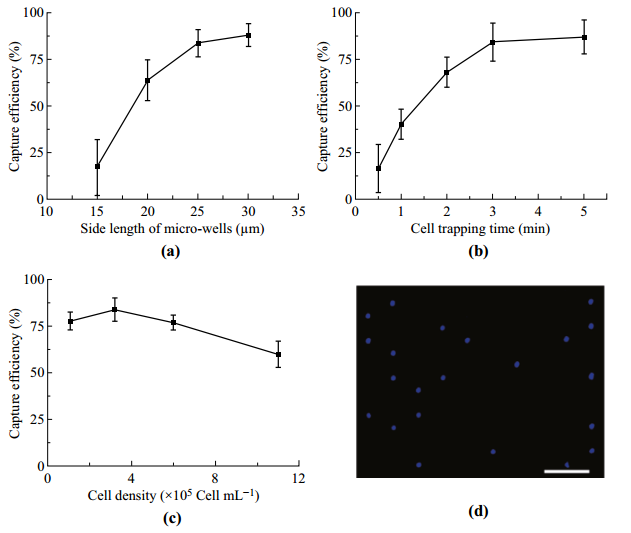
图3:细胞俘获效率的优化。捕获细胞的效率被定义为捕获的细胞与注入到微流控芯片中的所有细胞的比率。a)细胞捕获效率和方形微孔的边长之间的关系。b)细胞捕获效率与细胞捕获时间的关系。c) 细胞捕获效率和细胞密度的关系。d) 被困的单细胞用DAPI染色,呈现蓝色斑点。
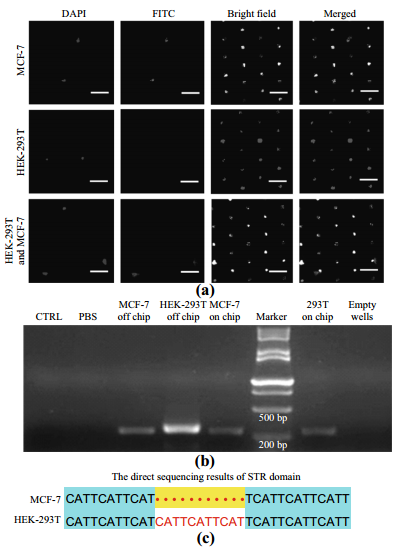 图4:荧光识别、扩增和测序MCF-7细胞。a)微孔细胞的荧光图像,上面一排是包含兼有DAPI(蓝色)和FITC(绿色)染色的MCF-7细胞的区域;中间一行只包含DAPI染色(蓝色)的HEK-293T细胞;较低行包含HEK-293T细胞和MCF-7细胞。b)琼脂糖凝胶荧光图像证实了STR结构域的DNA扩增产物。左两列空行和PBS的反应作为阴性对照;第三、第四左柱从纯HEK-293T和MCF-7细胞的产品,无切屑加工,作为阳性对照。三右列依次是不含细胞,只有HEK-293T细胞和MCF-7细胞的芯片产品。c)STR域测序结果的从细胞裂解物的区域到分别只包含HEK-293T和MCF-7细胞的区域。
图4:荧光识别、扩增和测序MCF-7细胞。a)微孔细胞的荧光图像,上面一排是包含兼有DAPI(蓝色)和FITC(绿色)染色的MCF-7细胞的区域;中间一行只包含DAPI染色(蓝色)的HEK-293T细胞;较低行包含HEK-293T细胞和MCF-7细胞。b)琼脂糖凝胶荧光图像证实了STR结构域的DNA扩增产物。左两列空行和PBS的反应作为阴性对照;第三、第四左柱从纯HEK-293T和MCF-7细胞的产品,无切屑加工,作为阳性对照。三右列依次是不含细胞,只有HEK-293T细胞和MCF-7细胞的芯片产品。c)STR域测序结果的从细胞裂解物的区域到分别只包含HEK-293T和MCF-7细胞的区域。
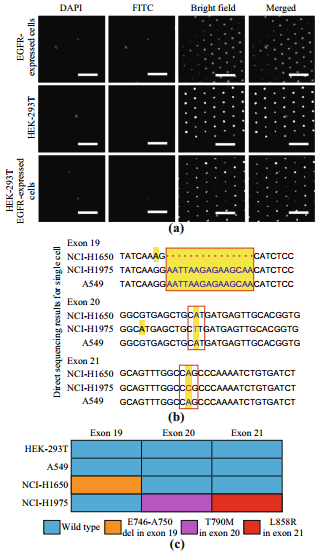
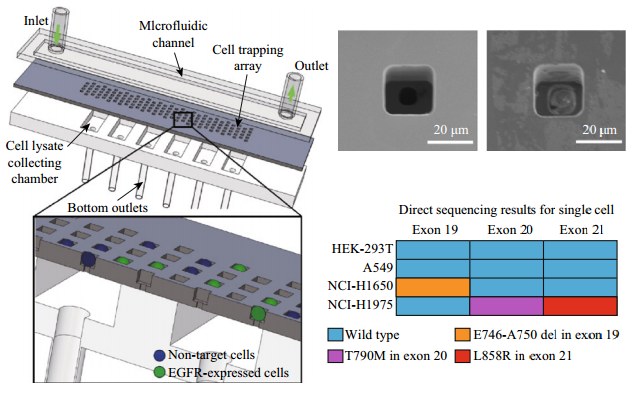
图5:检测EGFR多突变。a)微孔细胞的荧光图像,上面一排是只包含兼有DAPI(蓝色)和FITC(绿色)染色的EGFR信号细胞的区域;中间一行只包含DAPI染色(蓝色)的HEK-293T细胞;较低的行包含HEK-293T细胞和表皮生长因子受体表达的细胞。b)Sanger测序提供了准确信息:在外显子19,NICH1650细胞显示缺失突变(Del E746-A750);外显子20,NCI-H1975细胞株显示的点突变(T790M);外显子21,NICH1975细胞显示点突变(L858R)。c)对于NCI-H1975细胞株,在外显子20和21检测到突变;对NICH1650细胞,在外显子19检测到突变。此外,在HEK-293T或A549细胞无假阳性结果。
通讯作者简介

- 2010-12~现在 国家纳米科学中心 研究员
- 2007-04~2010-11 美国系统生物学研究所 研究科学家
- 2006-04~2007-04 美国系统生物学研究所 博士后
- 2005-04~2006-04 美国约翰霍普金斯大学 博士后
- 1995-06~1999-12 军事医学科学院 实习研究员
- 2000-04–2005-04 美国约翰霍普金斯大学 生物化学博士
- 1990-09–1995-06 复旦大学 遗传学本科
主要研究领域
- 探索纳米科学、基因组学和蛋白质组学的交叉前沿。
- 侧重利用纳米科学和系统生物学进行生物标志物的发现及临床应用
长按/扫描二维码阅读全文

关于我们
期刊简介
Nano-Micro Letters 是上海交通大学主办的英文学术期刊,主要报道纳米/微米尺度相关的最新高水平科研成果与评论文章及快讯,在 Springer 平台开放获取(open-access)出版。已被 SCI、Ei、SCOPUS、DOAJ、知网、万方等数据库收录,影响因子4.849。JCR学科分区在材料学科和物理学科均居Q1区。近年来,该刊入选“中国科技期刊国际影响力提升计划”和“上海市高水平高校学术期刊支持计划”项目资助,多次获得“中国最具国际影响力学术期刊”、 “高校百佳科技期刊奖”、“上海市高校精品期刊奖”、“优秀期刊网站奖”等荣誉。
期刊执行严格的同行评议,提供英文润色、图片精修、封面图片设计等服务。出版周期1-2个月 左右,高水平论文可加快出版。欢迎关注和投稿。
联系我们
Email:editorial_office@nmletters.org
Web:http://springer.com/40820
Tel.: 86-21-34207624
APP:nanomicroletters
Facebook: https://facebook.com/nanomicroletters
Twitter: https://twitter.com/nmletters
WeChat: nanomicroletters
QQ:100737456
nanomicroletters

长按 | 识别二维码 | 加关注
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 微流控芯片的医学应用:单细胞识别和检测突变表皮生长因子受体(EGFR)
 Nano-Micro Letters
Nano-Micro Letters 东南大学滕皋军院士、芮云峰、王乾乾教授等综述:肌肉骨骼系统中的微机器人
东南大学滕皋军院士、芮云峰、王乾乾教授等综述:肌肉骨骼系统中的微机器人 清华大学张萍、卢元等:“光虚拟芯片+人工智能”辅助的冠心病无创诊断
清华大学张萍、卢元等:“光虚拟芯片+人工智能”辅助的冠心病无创诊断