研究背景
当前,癌症已成为导致人类死亡的主要原因之一,且其患病率每年仍在持续攀升。尽管手术、化疗和放疗这三大传统癌症治疗方法已取得一定成效,但化疗和放疗不可避免地会对正常组织造成严重的不良影响,而手术具有创伤性。因此,开发一种高效、精确的无创治疗方法显得尤为迫切。随着科学技术的不断进步,光疗法,包括光动力疗法(PDT)和光热疗法(PTT),已取得了显著的发展。在PDT和PTT过程中,核心成分——光敏剂在特定波长的光照射下被激发,分别产生活性氧(ROS)和热量,以杀死肿瘤细胞。光疗因其时空选择性、无侵入性、不产生耐药性、副作用小等优点,展现出广阔的应用前景。然而,由于光的穿透深度有限,光疗仅限于治疗皮肤或浅表病变,这在一定程度上限制了其临床应用范围。
超声(US)作为一种机械波,凭借其卓越的组织穿透性,在腹部疾病诊断领域得到了广泛应用。近年来,其在心脏超声、妇产科检查以及血管内超声等方面均取得了显著进展,并在深部肿瘤的检测与治疗上展现出巨大的应用潜力。早在1989年,Umemura等人便发现,US照射联合血卟啉在体内外均表现出有效的抗肿瘤效果。这一效果源自血卟啉在超声的空化效应下被激活,进而产生具有细胞毒性的ROS。到1992年,Umemura等人提出了“声动力疗法”这一新型治疗概念。声动力疗法(SDT)作为一种新兴的无创治疗手段,是在PDT的基础上开发而来的。它主要涉及低强度超声和声敏剂的联合应用,其原理与功能与PDT颇为相似。相较于PDT、PTT等其他无创治疗方式,US具有更低的组织衰减和更深的穿透能力,能够触及深度超过10 cm的组织区域,这明显大于近红外(NIR)光在组织内的穿透深度。因此,SDT有望克服传统光疗在治疗深部肿瘤时所面临的局限性。此外,US在临床上被广泛认可为一种安全、有效的成像方式。因此,SDT在临床应用中展现出了广阔的前景。
尽管SDT在治疗多种癌细胞系的临床前研究中已展现出其治疗优势,但由于其机制尚未完全明确,其进一步的临床应用受到了限制。为了提升SDT在体内的抗肿瘤治疗效果并推动其临床转化,深入探究SDT的基本机制、设计合理的声敏剂递送系统以及充分利用SDT的特异性机制显得尤为重要。在SDT的过程中,声敏剂的选择同样起着至关重要的作用。由于传统的有机声敏剂存在水溶性低、肿瘤特异性差、早期清除率高等缺点,在肿瘤组织中的保留时间有限,从而影响了治疗效果。随着纳米技术的快速发展,各种纳米材料已被成功制备成声敏剂或声敏剂的纳米载体,极大地提高了声敏剂的积累。肿瘤微环境(TME)因肿瘤细胞的快速生长和代谢异常而呈现出酸性、缺氧和谷胱甘肽(GSH)水平升高的特征。此外,鉴于单一治疗方式的局限性,SDT通常与化学动力学治疗(CDT)、PTT和免疫治疗等协同作用,以进一步提升治疗效果。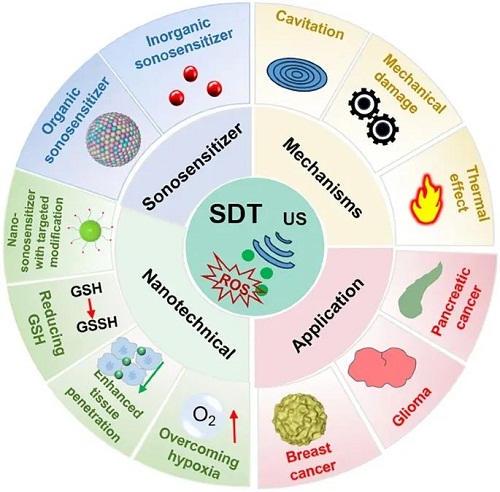
Nanomaterials Enhanced Sonodynamic Therapy for Multiple Tumor Treatment
Mengyao Yang, Xin Wang, Mengke Peng, Fei Wang, Senlin Hou*, Ruirui Xing*, Aibing Chen
Nano-Micro Letters (2025)17: 157
https://doi.org/10.1007/s40820-025-01666-8
本文亮点
1. 重点阐述了声动力疗法的主要机制及其临床应用潜力。
2. 纳米材料为增强癌症治疗效果提供了新的前景和发展方向。
3. 声动力疗法针对传统疗法难以达到的深部肿瘤治疗的最新发展,特别是对原位肿瘤。
内容简介
河北科技大学陈爱兵等人深入阐述了声动力疗法(SDT)的作用机制,并对纳米材料增强SDT的最新进展,特别是对原位肿瘤的SDT进行了全面的综述,旨在推动该领域的进一步发展。随后,介绍了有机和无机声敏剂等多功能声敏剂的合理设计和制造策略。SDT的治疗效果通常受到声敏剂固有结构和肿瘤微环境的阻碍,而纳米技术的进步为这一挑战开辟了新途径。本文着重探讨了纳米材料如何通过多种功能增强SDT的效果,具体涵盖以下几方面:增加病变部位声敏剂的积累,确保治疗的有效实施;借助图像引导技术的精确治疗,从而提高治疗安全性与精准度;减少肿瘤微环境中的抗氧化剂,以削弱其对SDT效果的负面影响;克服肿瘤微环境的缺氧状态。此外,还讨论了SDT与其他治疗方式,如化学动力学疗法及免疫治疗的结合,特别是对原位肿瘤的治疗。
图文导读
I 声动力疗法的作用机制
在深部肿瘤治疗领域,SDT超过了PDT所面临的穿透深度限制。低强度US的高穿透能力使其能够穿透深层组织,激活靶部位的声敏剂,产生大量的ROS。这一过程对肿瘤细胞产生毒性作用,同时最大限度地减少对邻近正常组织的损伤。当实验中加入ROS清除剂时,细胞死亡率显著下降,证明ROS是靶细胞死亡的主要原因。然而,在SDT过程中产生ROS的机制尚未得到明确的解释。目前,人们认为,SDT中ROS的产生主要是通过超声作用下的空化效应、超声发光和热解作用。此外,US引起的机械损伤和热效应也会对肿瘤细胞造成损伤(图1)。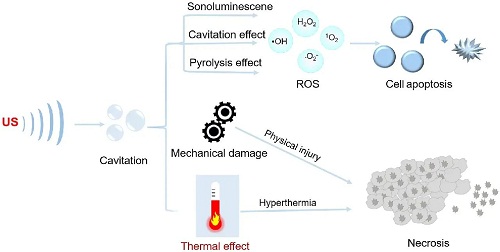
图1. SDT的主要作用机制。
II 声敏剂
声敏剂参与的声化学过程在SDT过程中起着重要作用。因此,SDT技术需要开发具有高声敏活性的新型声敏剂。目前,被广泛报道的声敏剂可分为有机声敏剂和无机声敏剂。与光敏剂类似,有机声敏剂主要是卟啉、酞菁及其衍生物,如原卟啉IX(PPIX)、二氢卟吩e6(Ce6)等等。此外,玫瑰孟加拉红(RB)、喹诺酮类、天然产物(如姜黄素)、一些化疗药物(如阿霉素)、吲哚菁绿(ICG)等也被发现有声敏感,而无机声敏剂主要指金属氧化物(如氧化银、氧化锌、二氧化钛等)和压电材料(黑磷、钛酸钡)。
2.1 有机声敏剂
有机声敏剂具有较强的结构调节性,可根据特殊需要进行设计和合成。由于有机光敏剂本身的结构存在疏水性等问题,直接应用简单的有机光敏剂分子往往导致治疗效果较差。Huang小组分别通过偶联单、二和四三乙烯二醇修饰锌(II)酞菁和青蒿琥酯单元设计了三种酞菁-青蒿琥酯偶联物(ZnPcT1A,ZnPcT2A和ZnPcT4A)(图2a)。这些共轭物在聚集形式下的声动力学ROS的产生明显高于非聚集形式。其中,ZnPcT4A表现出显著的性能,其在水中(聚集成纳米结构)的活性氧产量大约是添加2%聚氧乙烯蓖麻油的水中(纳米结构分解)的60倍(图2b)。声敏剂分子的聚集能力和聚集体的颗粒大小可以影响声动力学活性。此外,这种现象也可以在其他声敏剂上观察到,如ZnPcT4、Ce6和PpIX(图2c)。因此,他们提出,聚集增强的声动力学活性效应将是大多数有机声敏剂的常见现象。此外,体外和体内的研究都表明,ZnPcT4A聚集物具有较高的生物安全性和有效的SDT抗癌活性,肿瘤生长抑制率高达98%。本研究中发现的聚集增强声动力活性从根本上改变了在声敏剂设计中避免聚集的传统方法,从而为发展高效有机声敏剂开辟了新的途径。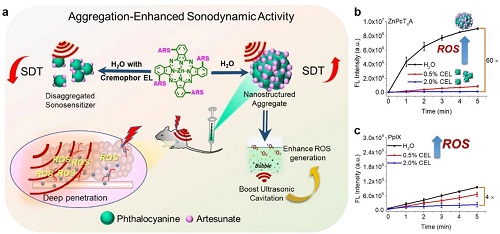
图2. 酞菁-青蒿琥酯偶联剂用于SDT。a.酞菁与青蒿琥酯的偶联,通过聚集表现出增强的声动力活性。b和c.以DCFHDA为荧光探针生成ROS。
2.2 无机声敏剂
虽然有机声敏剂已被证明在SDT中有效,但它们存在生物利用度低、稳定性差、合成复杂、水溶性差等缺点,这显著降低了US激活的声敏剂产生的ROS,抑制了处理效率。此外,大多数有机声敏剂来源于光敏剂,容易引起光毒性和皮肤过敏。近年来,无机声敏剂由于其优良的理化性质和多功能性而显示出巨大的SDT潜力,而限制其广泛应用的主要因素则是生物安全。目前,无机声敏剂的研究大多集中在抗肿瘤SDT的领域上。
氢化钛在储氢和高纯钛的制造中有广泛的应用。它表现出对光、超声和微波等外部刺激的响应性,当其多价钛元素受到刺激时,有利于光催化和声催化。然而,纳米级氢化钛在生物医学领域的应用迄今尚未见报道。Liu等人报道了通过液相剥离法制备纳米级金属氢化物(TiH1.924)的策略,剥离效率取决于剥离试剂与氢化物材料的表面能之间的相容性。随后的实验结果表明,所获得的TiH1.924纳米点在US暴露下可以产生ROS,表明其具有明显的声敏化效应。此外,这些TiH1.924纳米点表现出较强的NIR吸收,其温和的光热效应可以增强肿瘤血液生长,提高氧水平,从而使光热-声动力协同治疗(图3a)。此外,超小TiH1.924纳米点可以从体内去除,显著提高了其生物安全性,为金属氢化物纳米材料在生物医学中的广泛应用铺平了道路。
石墨烯量子点由于其独特的物理和化学性质,包括高稳定性、无毒性和优良的声敏感性,为SDT的发展提供了新的思路和方法。Ding和他们的合作者首次证明了N掺杂石墨烯量子点(N-GQDs)的优异声敏活性。N-GQDs暴露在US刺激下产生ROS的效率是传统超声敏剂的3-5倍(图3b)。本研究旨在阐明N掺杂碳纳米结构的声化学机理。实验和理论结果表明,N-GQDs中的吡咯N和吡啶N是声化学过程的反应位点。此外,由于吡咯N和吡啶N在石墨烯量子点晶格中的稳定性,即使对其肿瘤靶向修饰后,N-GQDs仍保持异常的声敏感活性。涉及氧化应激相关蛋白的其他检测显示,US照射下FA-N-GQDs产生的丰富ROS可通过PEX通路触发p53蛋白高表达的肿瘤细胞的氧化应激反应,最终通过p53蛋白促进肿瘤细胞凋亡(图3c)。细胞实验结果也表明,FA-N-GQDs暴露于US后的细胞杀伤率大于95%。此外,小鼠皮下肿瘤模型的治疗结果显示,FA-N-GQDs的靶向修饰可以快速稳定地在肿瘤组织中积累,在两次US照射后14天内肿瘤体积减少了95%以上。同时,由于FA-N-GQDs具有良好的稳定性和生物安全性,在治疗过程中未发现明显的毒副作用。
此外,Pan等人首次提出了“磷光声敏剂”的概念,设计并制备了一种新型的NIR磷光碳点,并将其应用于NIR成像介导的精确SDT肿瘤治疗。通过一步微波合成策略调节碳点的导电类型,制备的均质p-n结碳点不仅具有NIR磷光特性,而且具有增强的声动力活性(图3d)。最后,用同源靶向癌细胞膜包裹NIR磷碳点后,通过单次静脉注射,在荷瘤小鼠模型中可完全根除骨肉瘤。这项工作不仅为NIR成像介导SDT的应用开辟了一条新的途径,也为量子点荧光粉材料在近红外发光器件中的应用提供了一个新的思路。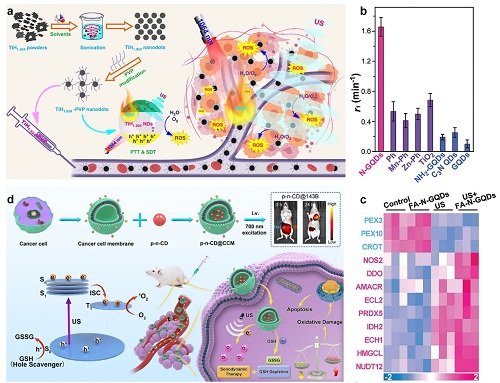
图3. a.用于SDT和PTT协同的TiH1.924纳米点的制备。 b.N-GQDs与传统声敏剂的声敏效果比较。 c.氧化应激相关蛋白,标示氧化应激反应。 d.p-n-CD@CCM的制备及SDT的应用。
III 纳米声敏剂增强SDT的治疗效果
虽然SDT引起了广泛的关注,但其治疗效率受到许多因素的影响,如声敏剂的固有结构,以及肿瘤微环境中的高GSH水平和缺氧环境。随着纳米技术的发展,纳米材料为增强癌症的治疗提供了新的前景和发展方向。鉴于上述问题,鉴于上述问题,基于纳米材料的各种构筑策略被实施以提高治疗效果。基于这些策略,将具有不同特性的纳米材料分为四类:增强肿瘤积累、成像引导、减少内源性抗氧化剂GSH和克服缺氧(表1)。
表1. 具有不同特性的纳米声敏剂制备策略总结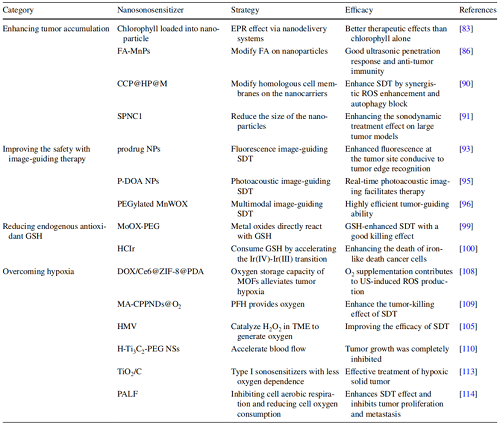
IV 声动力治疗在原位肿瘤中的应用
由于光的组织穿透能力较差,PDT仅限于治疗浅表癌或膀胱癌,而SDT利用US的穿透性能,可用于治疗更大或更深的肿瘤,从而实现精准治疗。这对于传统治疗方法难以达到的深部肿瘤,甚至是原位胰腺癌、神经胶质瘤等具有重要意义。此外,SDT与其他治疗方法的联合使用可以进一步提高治疗效果、肿瘤的靶向性和治疗的安全性。
4.1 胰腺癌
胰腺癌是最致命的癌症之一,其生存率非常低,近几十年来几乎没有改善。由于复杂的TME影响了各种治疗方法的有效性,胰腺癌的有效治疗仍然是面临的主要挑战。因此,迫切需要探索新的治疗方法或更有效的策略。SDT在多种类型肿瘤的治疗中显示出潜在的优势,特别是对于胰腺癌等深层肿瘤。
例如,Huang等人通过将2,2-偶氮唑[2-(2-咪唑啉-2-烷基)丙烷]盐酸(AIPH)载入缺氧反应的铜MOFs(Cu-MOF)中,开发了AIPH@Cu-MOF纳米颗粒(NPs)用来治疗原位胰腺肿瘤。在缺氧的TME中,AIPH@Cu-MOF NPs释放了Cu和AIPH。AIPH在US刺激下产生细胞毒性烷基自由基(图4a,b),而微环境中的GSH将Cu2⁺还原为Cu⁺,从而抑制GSH对ROS的消耗。此外,Cu⁺在弱酸性TME中能有效催化芬顿样反应,从而产生显著的ROS(图4c)。为了进一步验证AIPH@Cu-MOF NPs的协同增强作用,他们建立了原位胰腺肿瘤模型。通过检测小鼠的体重和肿瘤生长情况(图4d-f),明显发现Cu-MOF与对照组相比具有明显的肿瘤抑制作用,说明CDT在该胰腺癌模型中具有治疗效果。显著的是,在AIPH@Cu-MOF+US组的肿瘤生长抑制比在CuMOF+US组更明显,这表明AIPH偶联和随后暴露于US显著提高了这些MOFs的抗肿瘤活性。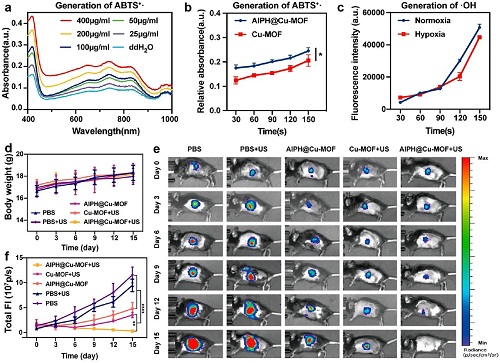
图4. AIPH@Cu-MOF治疗原位胰腺肿瘤。a.不同的AIPH@Cu-MOF浓度和b.US辐照下ABTS⁺的产生。c.AIPH@Cu-MOF生成·OH。Panc02-Luc原位荷瘤小鼠随时间变化的d.体重e.生物发光成像和f.荧光强度。
4.2 恶性胶质瘤
恶性胶质瘤作为颅脑原发性恶性肿瘤,预后差,复发率高,死亡率高,严重威胁人类的健康和生命安全。血脑屏障(BBB)由脑毛细血管内皮细胞、基底膜和神经胶质细胞足突组成,严重阻碍了药物传递。与PDT相比,SDT不仅具有穿透深层组织的特点,而且可以可逆地打开血脑屏障,增强药物向脑内的传递。
肿瘤细胞中还原性GSH的增加可以清除SDT产生的过量ROS,导致对肿瘤生长的抑制作用较差。此外,GSH的消耗可诱导GPX4失活,加速脂质过氧化,引发大量的铁凋亡。因此,构建具有协同GSH消耗和ROS产生能力的纳米声敏剂对于诱导铁凋亡和进行有效的肿瘤治疗至关重要。例如,Kang等人通过Cu2⁺离子与声敏化剂Ce6的配位自组装,构建了一个无载体的纳米粒子(Ce6@Cu NPs)。Ce6@Cu NPs的高效声动力效应协同诱导原位胶质瘤铁凋亡和铜凋亡(图5a)。Ce6@Cu NPs被U87MG细胞摄取后,在超声照射下表现出良好的声动力效应,产生大量的1O₂(图5b)。这导致了多不饱和脂肪酸的氧化,然后引发了致命的脂质过氧化。此外,Ce6@Cu NPs有效地消耗了肿瘤细胞中过量产生的GSH(图5c),导致GPX4失活(图5d),加速脂质过氧化和不可逆的铁凋亡。由于Cu2⁺与还原性GSH反应,U87MG细胞中Cu⁺浓度显著升高,导致铁氧还蛋白-1和LIAS的表达下调(图5e)。这一过程显著促进了脂酰化二氢脂酰胺S-乙酰转移酶的寡聚化,触发蛋白质毒性应激,最终导致细胞破裂。重要的是,Ce6@Cu NPs表现出令人满意的穿透血脑屏障的能力,并在原位U87MG-Luc胶质母细胞瘤中显著富集(图5f)。Ce6@ Cu NPs的SDT协同诱导铁凋亡和铜凋亡已在体内和体外均得到了证实,且没有副作用。本研究不仅为恶性胶质瘤的治疗提供了一种无载体的纳米声敏剂,而且提供了一种基于协同铁凋亡和铜凋亡的有前途的肿瘤治疗策略。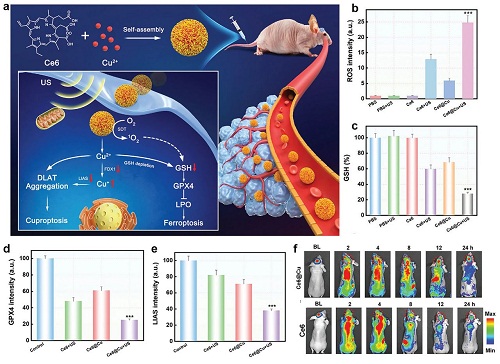
图5. a.Ce6@CuNPs的制备并用于声动力增强原位胶质母细胞瘤的铜凋亡和铁凋亡。b.以DCFHDA为荧光探针,测定U87MG细胞中生成ROS。c.用不同样品处理U87MG细胞的GSH水平。不用样品处理U87MG细胞中d GPX4和e LIAS的相应定量。f.原位U87MG-Luc荷瘤小鼠静脉注射不同样品后的体内荧光成像。
4.3 乳腺癌
TNBC具有丰富胶原纤维的致密基质,形成屏障,限制纳米材料向肿瘤实体的传递,并阻止细胞毒性T淋巴细胞(CTL)的肿瘤侵袭。因此,开发一种能够促进治疗性纳米材料和CTLS在肿瘤中的渗透的策略,对TNBC的治疗具有重要意义。SDT作为一种新兴的无创、高度可控、深度渗透的肿瘤治疗策略,为TNBC的治疗提供了一种新的途径。在临床应用方面,Inui等报道了一例55岁女性复发性乳腺癌。经修饰锡Ce6和5-ALA介导的SDT后,巨噬细胞活化(Gc蛋白来源的巨噬细胞激活因子,GcMAF)和激素治疗(依西美坦)、右肺胸膜灌注和胸膜内结节性肿瘤完全消失。开发新型低带隙纳米声敏剂是提高ROS的产生,从而提高其抗肿瘤能力的必要条件。此外,使用纳米声敏剂克服肿瘤基质屏障并穿透肿瘤内部是提高SDT肿瘤治疗结果的有效策略。
SDT作为一种很有前途的无创性肿瘤治疗方法,其治疗能力一直因ROS产率受肿瘤的缺氧微环境限制而受到阻碍。Pan等人利用酞菁介导的热解策略,开发了一种具有五配位结构的碳纳米框架限定N配位锰单原子声敏剂(MnN5SA/CNF)(图6a)。与传统的四配位锰(MnN4SA/CNF)和二氧化锰相比,MnN5SA/CNF具有较好的声动力活性和显著较高的多酶样催化活性,克服了缺氧的肿瘤微环境,从而显著提高了SDT的活性(图6b)。这主要归因于优化的配位结构和缺陷增强的空化效应,五正酸结构使Mn的d带中心从−0.547 eV降低到−0.829 eV,增强了含氧中间体的解吸能力,从而加速了催化过程。最后,将MnN5SA/CNF应用于原位乳腺癌小鼠模型。图6c,d验证了有效的肿瘤抑制率达到了94.43%,而图6e验证了MnN5SA/CNF对正常组织几乎没有损伤。这种对声敏剂的协调调节策略代表了SDT的重大进展。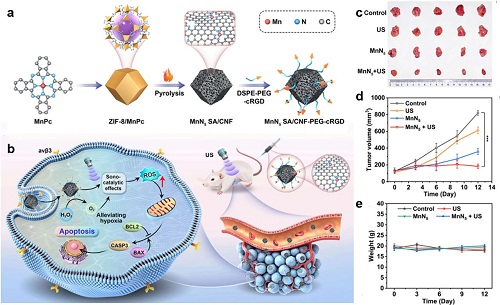
图6. MnN5SA/CNF治疗原位乳腺癌。a.MnN5SA/CNF的制备示意图。b.用于SDT的MnN5SA/CNF。c.肿瘤的光学照片。d.肿瘤体积生长曲线。e.各种治疗后的小鼠体重。
V 总结
SDT作为一种新兴的治疗方式,具有非侵入性、时空可控性、高治疗效果、深度组织渗透、促进药物传递等优点,是一种极有前途的治疗方式。然而,SDT的作用机制尚未得到明确的解释。目前,提出的机制主要包括超声空化效应、机械和热损伤。最被广泛接受的机制是通过声敏剂或空化效应触发ROS的产生。因此,有必要进一步总结SDT的作用机理,为改进SDT提供直接的理论依据。声敏剂是SDT的核心组成部分。虽然已经开发了多种声敏剂,并表明了其在生物医学应用中SDT的可行性,但其临床应用面临着许多挑战。纳米声敏剂为克服TME的障碍提供了帮助,并且可以根据各种肿瘤特性进行定制和修饰,使声敏剂能够更好地适应治疗的特殊需求。例如,血脑屏障在胶质母细胞瘤的治疗中构成了一个明显的障碍。幸运的是,纳米材料的EPR效应可以有效地促进药物通过血脑屏障的运输,从而提高了它们在大脑中的富集。其次,可以在纳米声敏剂的表面引入特殊的修饰,如连接靶向配体(如转铁蛋白受体抗体)。这些配体可以选择性地与血脑屏障上相应的受体结合,使声敏剂能够靶向传递。本文总结了近年来纳米技术辅助声敏剂在SDT中的应用。采用不同的策略通过肿瘤的积累,提高成像引导治疗的安全性,减少内源性抗氧化剂,如谷胱甘肽,以及克服乏氧微环境来提高SDT的效果。此外,SDT比PDT具有更深的组织穿透能力。因此,它在不同类型的癌症中有更好的表现。
尽管研究人员在设计和构建安全有效的新型声敏剂方面取得了相当大的努力,并在临床前研究中取得了许多有希望的结果,但其成功转化为临床实践,仍存在几个关键问题和挑战。这些包括SDT的作用机制、SDT的评价、声敏剂分子的毒副作用、超声设备和复杂的制备技术(图7)。因此,未来的研究应更加关注:
1. 明确SDT的作用机制,包括生物毒性和治疗效果。这将有助于构建切合实际的SDT介导的治疗方法,并为今后声敏剂的合理设计提供方向。
2. 为SDT制定具体的评估方法。目前还没有全面的方法来评价SDT的效果,主要是通过测量产生ROS的能力来估计,对于空化效应也没有可比的评估方法。因此,制定一套评价声敏剂和SDT相关性能的指南是很重要的。
3. 开发新的声敏剂分子。目前,研究最广泛的声敏剂分子仍然是光敏剂,但这些分子大多会引起严重的光毒性和不良副作用。因此,迫切需要设计和合成安全、高效、低光毒性、高灵敏度、高肿瘤选择性的声敏剂。
4. 设计先进的超声波设备。SDT的成功实施依赖于超声设备,但目前的超声设备只适用于小鼠体内和体外的研究,而不是用于人体的临床治疗。由于人类和小鼠之间在组织、骨骼和其他方面的差异,人类的临床治疗需要具有更高强度的US。先进的设备能够优化超声波参数,以确保其在临床实践中的可行性和实用性。因此,需要更先进的超声设备来同时执行多种功能,这对提高SDT的工作效率至关重要。
5. 优化纳米声敏剂。虽然纳米材料可以通过不同的策略修饰来提高声动力治疗的疗效,但在临床转化中它们仍然面临着几个关键的技术挑战。首先,纳米材料在生物环境中的稳定性受到生物分子的影响,这反过来又影响了它们的声敏活性。此外,安全性评估是纳米材料临床应用前不可或缺的一步。然而,大多数纳米声敏剂具有复杂的结构,缺乏生物相容性和生物降解性,严重阻碍了它们的大规模生产和进一步应用。因此,优化纳米材料制备的简单性,提高纳米材料的稳定性和生物安全性,实现最有效、相互强化的协同效应,有助于进一步推进其临床应用。
图7. 未来SDT的发展前景示意图。
随着科学的前沿发现和创新,相信上述问题将在不久的将来得到解决,而SDT将在癌症的临床治疗中发挥重要作用。
作者简介

关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2023 JCR IF=31.6,学科排名Q1区前3%,中国科学院期刊分区1区Top期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 河北科技大学陈爱兵等人综述:纳米材料增强声动力疗法对多种肿瘤的治疗
 Nano-Micro Letters
Nano-Micro Letters 北航胡明俊&北京纳米能源所杨军等:超稳定/高比能量/宽温域水系碱性钠离子电池通过采用微孔 C₄N/rGO 阳极实现
北航胡明俊&北京纳米能源所杨军等:超稳定/高比能量/宽温域水系碱性钠离子电池通过采用微孔 C₄N/rGO 阳极实现 山大李阳等:一种基于水凝胶的柔性集成多模态传感贴片
山大李阳等:一种基于水凝胶的柔性集成多模态传感贴片 东南大学赵远锦等综述:具有靶向功能mRNA纳米药物的开发
东南大学赵远锦等综述:具有靶向功能mRNA纳米药物的开发 宾州州立大学程寰宇&高丽大学Suk-Won Hwang等:无线、多功能系统集成可编程软体机器人
宾州州立大学程寰宇&高丽大学Suk-Won Hwang等:无线、多功能系统集成可编程软体机器人