研究背景
骨组织是人体的重要组成部分,是为运动提供必要支持的基本器官系统之一,在促进身体活动方面发挥着关键作用。近年来,大约 50% 的成年人,尤其是老年人,会经历骨损伤或缺损,这些问题通常由创伤、疾病等因素引起,给人们生活带来巨大的痛苦和不便。骨修复的临床治疗方法主要包括自体移植、同种异体移植和内固定。虽然这些方法已被广泛接受,但在临床应用中的缺点也显而易见,例如,供体组织有限、移植过程存在感染、潜在免疫原性的风险和其他相关问题。截止目前,各种生物活性分子,包括药物、生长因子、干细胞、细胞外囊泡和生物活性离子,已经被直接应用于受损的骨组织,并表现出令人满意的治疗效果。然而,其体内稳定性低和病变部位滞留能力差的缺点可能需要高剂量使用生物活性分子,从而增加对正常组织的毒性,并有可能产生多重耐药性。基于此,水凝胶通常可以降低与药物定向输送相关的潜在毒性和副作用,同时还可以通过其在体内缓慢的生物降解性和溶胀特性延长局部药物的保留率,再者水凝胶具有多功能刺激响应特性,可由各种因素触发,进而确保了生物活性分子从水凝胶网络中可控释放,避免了治疗剂的不必要浪费。基于水凝胶的空间/顺序输送与自然骨愈合过程相结合是一种有前途的骨修复策略。

Recent strategies and advances in hydrogel-based delivery platforms for bone regeneration
Xiao Wang, Jia Zeng, Donglin Gan, Kun Ling, Mingfang He*, Jianshu Li*, Yongping Lu*
Nano-Micro Letters (2025)17: 73
https://doi.org/10.1007/s40820-024-01557-4
本文亮点
1. 本文总结了纳米/微米级载体和水凝胶网络相结合的递送平台用于骨修复。
2. 本文介绍了生物活性分子在不同外界刺激下(包括近红外光、温度改变、超声以及炎症环境等)的递送策略(包括纳米颗粒、纳米片和微球等)。
3. 本文讨论了纳米/微米级载体复合的水凝胶基递送平台在临床转化和发展方面的前景和挑战。
内容简介
生物活性分子在调控多种骨形成的进程中已展现出巨大的潜力,这使得其在骨修复领域大放异彩。但是,生物活性分子的广泛应用却受其在体内低富集和短半衰期的缺陷所限制。作为一种理想的载体,水凝胶可以延长生物活性分子在病灶处的滞留时间和半衰期,同时避免暴释,进而减少副作用,最后促进其在生理环境中被机体有效吸收发挥作用。广元中心医院鲁永平、何明方&四川大学李建树等系统性地总结了用于骨修复的负载生物活性分子水凝胶的近展,主要聚焦于颅骨缺损修复、股骨缺损修复、牙周骨再生以及各种基础病下的骨再生。此外,本文讨论了用于改善生物活性分子递送行为的现有策略,例如,刺激响应性递送、载体辅助递送以及序次递送。最后,本文阐述了现有水凝胶负载生物活性分子在骨再生领域中所存在的挑战和未来发展方向。
图文导读
I 水凝胶体系促进生物活性因子递送的策略
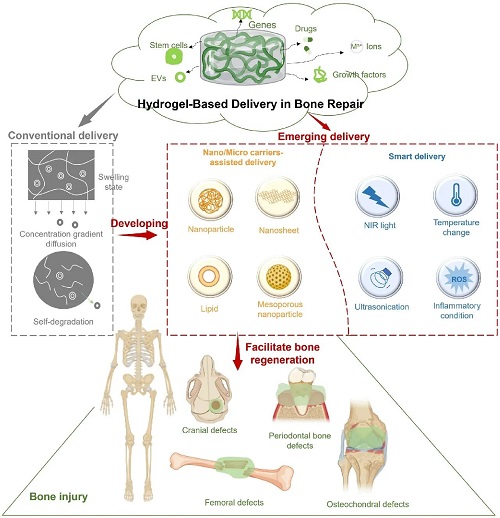
图1.水凝胶基递送平台用于骨再生。常见骨损伤主要包括颅骨缺损、股骨缺损、牙周骨缺损以及骨-软骨缺损,传统水凝胶通过其本征生物降解性和(或)溶胀性递送生物活性分子至骨缺损处,进而实现骨再生进程。新兴的递送体系利用水凝胶作为基质在纳米/微米级载体、外界刺激以及分层结构的辅助下用于药物递送。
II 水凝胶基递送策略用于骨再生
2.1 传统递送策略
介绍了水凝胶递送生物活性因子在颅骨、股骨/髌骨、牙周骨、骨-软骨及软骨缺损修复中的应用。
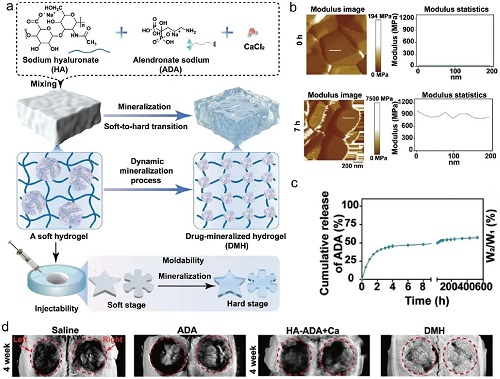
图2. a)DMH水凝胶的合成与动态矿化过程。b)DMH水凝胶在0小时和7小时的杨氏模量和模量统计。c)37℃下水凝胶在PBS溶液中释放ADA的释放曲线。d)对比第四周DMH水凝胶和空白组治疗颅骨缺损的效果。
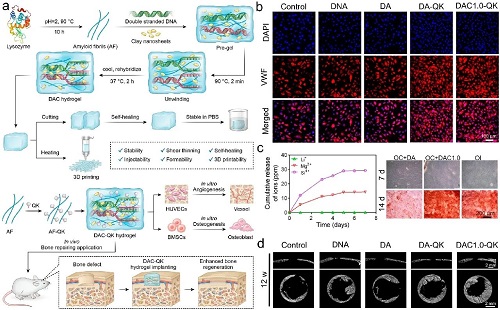
图3. a)DAC水凝胶的制备、多功能性以及骨缺损修复能力。b)HUVECs和VWF蛋白(红色)的免疫荧光染色,细胞核为蓝色。c)在不同时间下,水凝胶中生物活性离子的释放曲线;利用提取培养基培养BMSCs 7天和14天的茜素红染色。d)水凝胶治疗后颅骨缺损的横截面和纵向micro-CT。
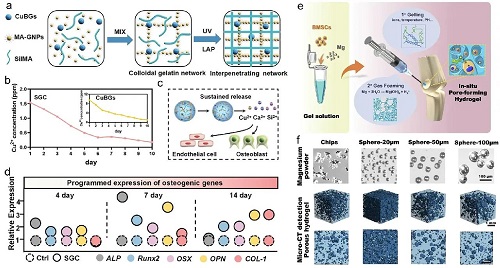
图4. a)通过双重光交联策略制备具有互穿网络的SGC水凝胶。b)铜离子分别从CuBG和SGC水凝胶中释放的释放曲线(超过10天)和示意图。c)SGC水凝胶促血管生成和骨生成的机制。d)不同时间下,SGC水凝胶对各种骨形成相关基因表达水平的调控作用。
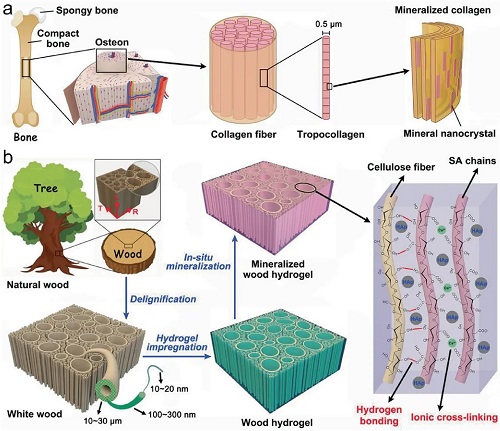
图5. 矿化木基水凝胶的设计策略、制备流程以及微观结构示意图。
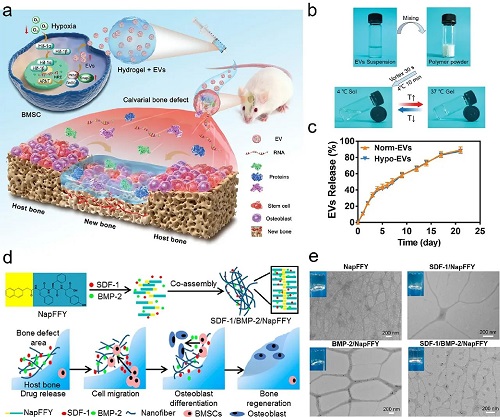
图6. a)负载Hypo-EVs的PEG/聚多肽水凝胶促进颅骨再生。b)PEG/聚多肽水凝胶在37℃快速成胶。c)PEG/聚多肽水凝胶释放EVs的释放曲线。d)负载SDF-1/BMP-2的NapFFY水凝胶网络用于牙周骨修复。e)SDF-1和BMP-2在NapFFY水凝胶网络中的分布情况。
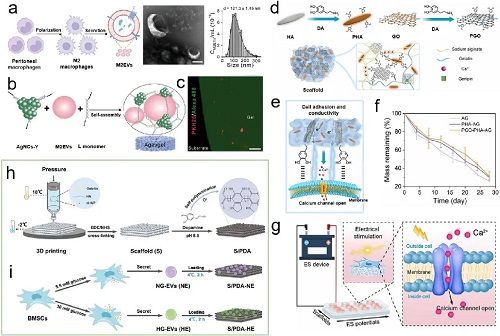
图7. a)M2EVs的制备流程、微观形貌和颗粒尺寸。b)Agevgel水凝胶封装M2EVs的示意图。c)M2EVs在Agevgel水凝胶网络中的分布情况。M2EVs和AgNCs分别用PKH26和Alex Fluor染色。d)PGO-PHAp-AG支架的制备示意图。e)钙离子从PGO-PHAp-AG支架中的释放过程。f)不同支架在PBS-II型胶原酶溶液中的降解曲线。g)高通量电刺激促进PGO-PHAp-AG支架释放钙离子进入细胞,进而加速骨形成。3D打印支架Gel/HA/nHAp的h)制备以及i)负载EVs过程。
2.1 新型递送策略
2.1.1 纳米/微米载体用于生物活性因子递送
介绍了负载纳米材料、微球及工程化囊泡的水凝胶递送生物活性因子在骨修复中的应用。
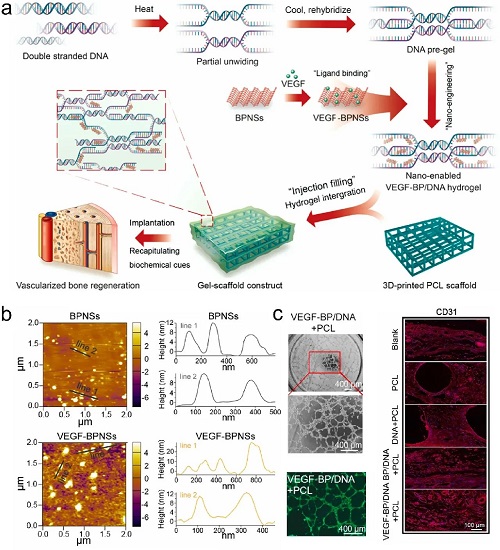
图8. a)用于血管化骨再生的DNA水凝胶制备示意图。b)BPNSs和VEGF-BPNSs的原子力显微镜图片。c)DNA水凝胶在体外促进HUVECs形成管,在体内促进血管的形成。
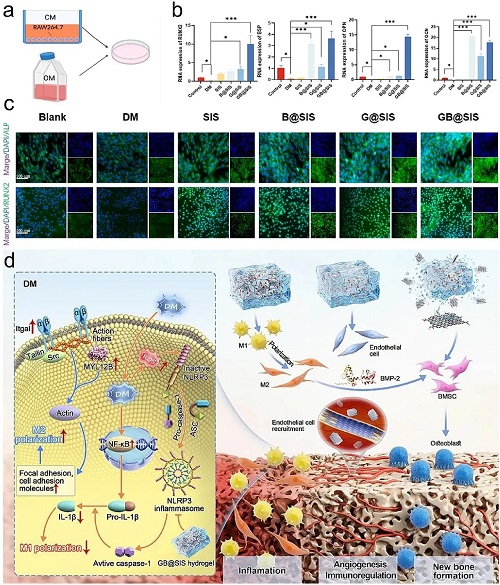
图9. a)混合培养基(包含培养巨噬细胞培养基和骨生成诱导培养基)的示意图。b)在成骨免疫调节环境下,对比不同材料对培养BMSCs14天后骨再生相关基因表达水平的调控作用。c)BMSCs培养7天后,ALP和RUNX2的免疫荧光染色图片。d)水凝胶递送系统促进新骨形成的机制。
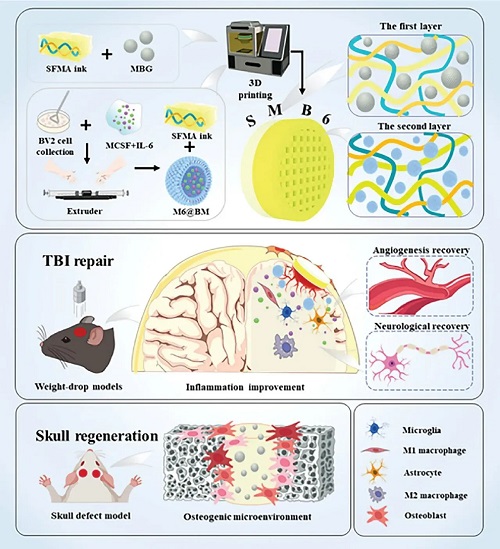
图10.仿生颅骨-脑水凝胶贴片促进TBI和颅骨缺损一体化修复。
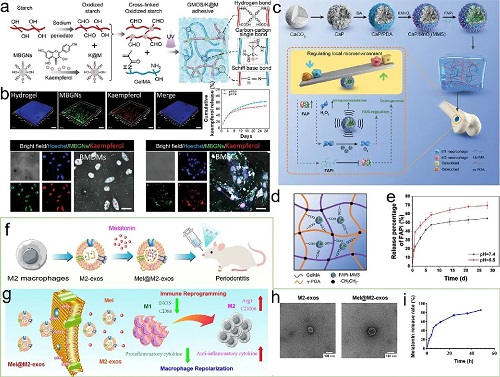
图11. a)山柰酚修饰GMOS/K@M水凝胶的制备。b)山柰酚在水凝胶网络中的分布情况和释放曲线。c)负载FAPi的MnO2-CaP微球复合水凝胶用于骨松环境下骨组织再生。d)负载FAPi微球与水凝胶聚合物链之间的相互作用。e)复合水凝胶释放FAPi的释放曲线。f)负载Mel工程化外泌体GelMA水凝胶用于牙周骨缺损治疗。g)外泌体释放Mel促进免疫调控进程。Mel工程化外泌体的h)扫描电镜图片以及i)释放Mel的释放曲线。
2.1.2 水凝胶的智能递送策略
光热响应递送
介绍了光热相应性水凝胶递送生物活性因子在骨修复中的应用。
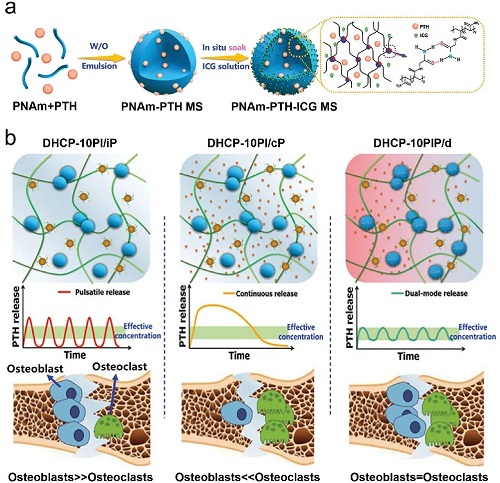
图12. a)利用水/油乳液制备具有近红外响应特性的PIP微球。b)成骨细胞和破骨细胞在不同释放行为下的活动情况。
超声响应递送
介绍了超声响应性水凝胶递送生物活性因子在骨修复中的应用。
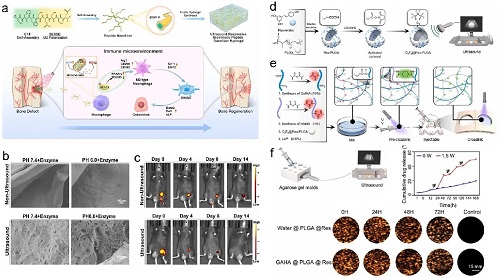
图13. a)负载肽纳米纤维的水凝胶制备过程以及其在超声刺激下促进骨形成的机制。b)负载肽纳米纤维水凝胶在超声条件或无超声条件下的扫描电镜图片。c)超声刺激促进水凝胶在体内降解。d)Res修饰纳米气泡过程以及e)纳米气泡复合水凝胶用于颅骨缺损修复。f)复合水凝胶在超声刺激下释放Res的实验设计和释放曲线。
炎性环境响应递送
介绍了炎性环境响应性水凝胶递送生物活性因子在骨修复中的应用。
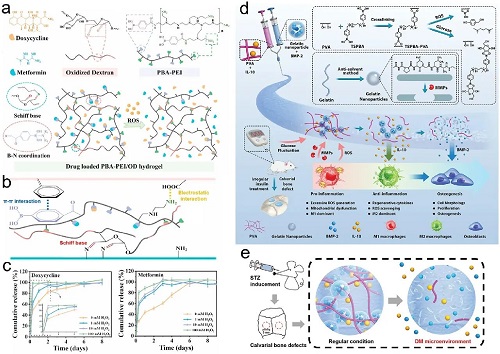
图14. a)制备负载Doxy和Met的PBA/PEI/OD水凝胶的流程图以及ROS响应水凝胶的降解示意图。b)水凝胶对组织的粘附机制。c)Doxy和Met的累计释放曲线。d)负载BMP-2和IL-10的ROS响应水凝胶的制备。e)糖尿病所处微环境下水凝胶递送BMP-2和IL-10。
时序性递送
介绍了水凝胶时序性递送生物活性因子在骨修复中的应用。
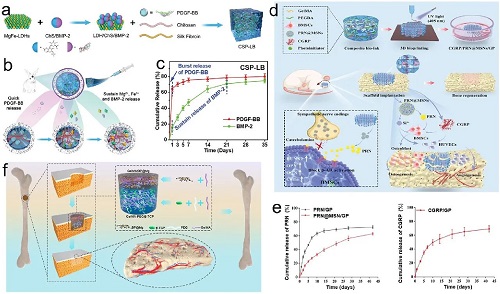
图15. a)基于MgFe-LDH纳米片封装BMP-2和PDGF-BB的水凝胶制备。病灶处,PDGF-BB暴释和BMP-2持续释放b)示意图及c)曲线。d)MSNs负载PRN后将其引入至CGRP复合GelMA/PEGDA水凝胶中,进而重构神经调节免疫微环境用于颅骨缺损修复。e)PRN和CGRP的释放曲线。f)双层水凝胶(骨膜修复层GelMA-BP@Mg水凝胶和骨修复层GelMA-PEG/β-TCP水凝胶层)重构神经-血管网络。
III 总结
骨愈合涉及漫长而复杂的过程,涉及分子和细胞信号通路之间的多种相互作用。这些通路受各种生物活性分子的调节,例如药物、生长因子、生物活性离子和囊泡。在骨损伤部位积累足够的生物活性分子可以确保骨再生过程顺利进行。然而,由于生物活性分子在生理条件下具有低滞留性,直接将生物活性分子应用到骨损伤部位会导致负面影响,例如生物利用度低和潜在的副作用。近几十年来,水凝胶基递送平台因其独特的性能和多功能特性而成为骨再生领域的热点研究。这些递送平台表现出一系列理想的特性,包括由于其类组织结构、特性而具有的稳定性,从而延长生物活性分子在体内的高生物活性和有效时间。此外,水凝胶基递送系统能够在伤口部位原位持续释放生物活性分子,提高药物利用效率,从而降低医疗成本。此外,它们可以实现生物活性分子的顺序和响应性释放,以满足骨愈合各个阶段的要求。
作者简介

本文通讯作者
针对组织修复的生物医用水凝胶复合材料的构建与应用以及纳米药物递送系统相关的研究。

本文通讯作者

本文通讯作者
关于我们

Nano-Micro Letters《纳微快报(英文)》是上海交通大学主办、在Springer Nature开放获取(open-access)出版的学术期刊,主要报道纳米/微米尺度相关的高水平文章(research article, review, communication, perspective, highlight, etc),包括微纳米材料与结构的合成表征与性能及其在能源、催化、环境、传感、电磁波吸收与屏蔽、生物医学等领域的应用研究。已被SCI、EI、PubMed、SCOPUS等数据库收录,2023 IF=31.6,学科排名Q1区前3%,中国科学院期刊分区1区期刊。多次荣获“中国最具国际影响力学术期刊”、“中国高校杰出科技期刊”、“上海市精品科技期刊”等荣誉,2021年荣获“中国出版政府奖期刊奖提名奖”。欢迎关注和投稿。
Web: https://springer.com/40820
E-mail: editor@nmlett.org
Tel: 021-34207624
如果文章对您有帮助,可以与别人分享!:Nano-Micro Letters » 四川大学李建树等综述:水凝胶递送平台用于骨修复
 Nano-Micro Letters
Nano-Micro Letters 徐卫林院士、万骏&港中文龙祎等: 中红外透明材料的结构主导机制与光子能量调控
徐卫林院士、万骏&港中文龙祎等: 中红外透明材料的结构主导机制与光子能量调控 西工大马晓燕等:仿生纳米纤维管束复合膜用于高效离子传输与稳定全固态锂电池
西工大马晓燕等:仿生纳米纤维管束复合膜用于高效离子传输与稳定全固态锂电池 华师大施国跃、张闽等:模块化智能微针平台开启机器学习驱动的个性化健康监测新时代
华师大施国跃、张闽等:模块化智能微针平台开启机器学习驱动的个性化健康监测新时代 徐卫林院士&陈凤翔等综述:无机高性能纤维基电磁屏蔽材料—从界面调控到多功能集成
徐卫林院士&陈凤翔等综述:无机高性能纤维基电磁屏蔽材料—从界面调控到多功能集成